| Новости | e-Образование | Врачебные Общества | Тематические группы | Библиотека | Медиатека | Мероприятия | Атлас |
Присоединяйтесь!
- Повышение квалификации
- Сертифицированное образование
- Актуальные статьи
- Обзоры и репортажи
- Клинические случаи
- Новости медицины
- Советы коллег
Сообщество: Педиатрическое Респираторное Общество
Эффективная защита слизистой носа у больных аллергическим ринитом. Обзор по препарату Назаваль
Н.М.Ненашева, канд. мед. наук, профессор кафедры клинической аллергологии ГБОУ ДПО РМАПО, г. Москва
Аллергический ринит (АР) – это воспалительное заболевание, в основе которого лежит аллергическая IgE-обусловленная реакция, развивающаяся в слизистой носа в ответ на воздействие аллергенов окружающей среды, и проявляющееся ринореей, чиханием, зудом в носу, нарушением носового дыхания и, зачастую, обоняния.
АР одно из наиболее распространенных заболеваний человека, встречающееся практически во всех странах мира и поражающее от 15 до 40% лиц всех возрастов, только в Европе 30% населения страдают АР (1,2). В РФ от 7 до 13% больных АР (3).
АР не относится к числу тяжелых заболеваний, однако он является причиной существенного снижения качества жизни больных, нарушения сна, ограничений в обучении и профессиональной деятельности. Кроме этого, важность проблемы АР обусловлена его тесной связью с такими заболеваниями, как бронхиальная астма (БА), острый и хронический риносинусит, аллергический конъюнктивит. Установлено, что у 24% детей аллергический ринит явился предрасполагающим фактором для развития острого и хронического среднего отита, а в 28% случаев – хронического риносинусисита (1). БА значимо чаще развивается у больных АР, а симптомы ринита присутствуют более, чем у 80% больных БА (2,4). Таким образом, медико-социальное значение аллергического ринита обусловлено его широкой распространенностью, влиянием на качество жизни больных, способностью ухудшать течение БА и часто предшествовать ее развитию (у 32-49% больных) и влиять на развитие других заболеваний ЛОР-органов.
Большинство пациентов с АР могут иметь контролируемое течение заболевания в результате применения терапии, одобренной международными и национальными руководствами и, как правило, включающей следующие основные этапы: предупреждение контакта с аллергеном; фармакотерапию; специфическую иммунотерапию; и обучение пациента. Основными видами фармакотерапии АР является применение оральных и топических антигистаминных препаратов, интраназальных кортикостероидов (ИнГКС), кромонов, антилейкотриеновых препаратов и деконгестантов.
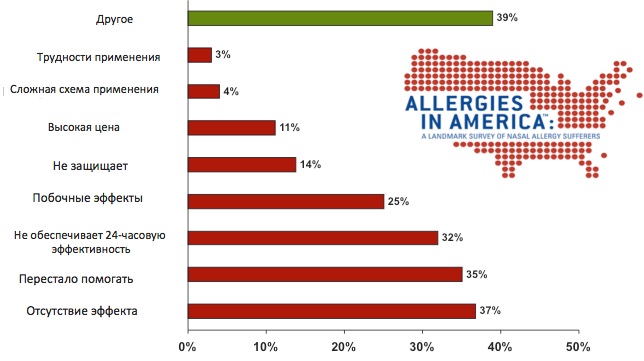
Однако до 20% больных с средне-тяжелыми и тяжелыми симптомами АР, комплаентных к назначенной терапии, продолжают страдать от АР (5). Кроме того, аллергический конъюнктивит часто ассоциирован с сезонным АР и существенно труднее поддается контролю, чем симптомы ринита (6). Неэффективность фармакотерапии является одной из основных причин отказа от терапии среди пациентов с АР, как показало исследование, проведенное в США (Рис.1).
В связи с этим, актуальным является поиск новых методов лечения и профилактики АР. Относительно недавно (в 1994 г.) в Англии был предложен для этой цели инертный порошок целлюлозы - препарат Nasaleze или Назаваль, который в настоящее время успешно применяется уже в 50 странах.
Характеристика Назаваля и механизм действия
Назаваль представляет собой микродисперсный порошок целлюлозы в спрее-дозаторе. Механизм его действия заключается в защите слизистой носа от попадания в организм аэроаллергенов (пыльцы растений, бытовых аллергенов, эпидермальных аллергенов животных и птиц) и других аэрополлютантов, попадающих в носовую полость при вдыхании воздуха.
Микродисперсный порошок целлюлозы из спрея-дозатора попадает на слизистую носовых ходов, связывается со слизью и образует прозрачный гелеобразный слой, который выстилает носовую полость и служит естественным барьером против проникновения аэроаллергенов и поллютантов в организм, таким образом, препятствуя развитию аллергической реакции (Рис.2). В последующем этот гель выводится, благодаря работе мукоциллиарного аппарата.
Рис.1. Причины, по которым пациенты прекратили принимать лекарственные препараты для лечения АР (17).
Целлюлозная добавка, в том числе, порошок целлюлозы является безопасным для здоровья, разрешен в странах ЕС (Е 460) и широко применяется в пищевой, кондитерской и медицинской промышленности, в качестве носителя, стабилизатора, регулятора влаги, наполнителя или разделителя, причем для большинства продуктов питания без ограничения количества. Порошок целлюлозы обладает умеренным бактерицидным действием, однако не является лекарственным препаратом, поэтому Назаваль не является лекарством, а представляет собой защитное медицинское средство, высокого 1 класса безопасности, пригодное для длительного использования.
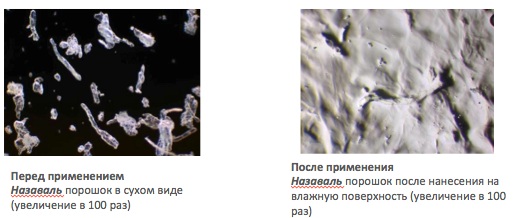
Рис.2 Микродисперсный порошок целлюлозы из спрея-дозатора попадает на слизистую носа, связывается со слизью и образует прочную гелеобразную пленку, которая выстилает носовую полость.
Важным свойством Назаваля является то, что средний размер микрочастиц целлюлозы составляет 118 мкм (от 5 до 500 мкм), что позволяет им проникать только в носоглотку, не достигая трахеи, бронхов, бронхиол и альвеол, ибо размер респирабельных частиц, способных достичь нижних дыхательных путей, должен быть меньше 5 мкм. Гелеобразная пленка, образуемая микродисперсным инертным порошком растительной целлюлозы, довольно легко удаляется при высмаркивании, поэтому после каждого очищения полости носа требуется повторное применение Назаваля. Элиминация, образуемой Назавалем, защитной пленки в результате мукоциллиарного транспорта, являлась одним из критических моментов в характеристике препарата. Однако в исследовании Diethart B. и коллег (7) было убедительно показано, что образование гелеобразной пленки порошком гидроксипропилметилцеллюлозы приводит к выраженному снижению скорости мукоциллиарного клиренса. Аппликация 10 мг микродисперсной целлюлозы приводит к удлинению времени мукоциллиарного клиренса с 11,14 мин до 35,45 мин (р<0,0005); 20 мг – удлиняют это интервал до 50,37 мин. Таким образом, была продемонстрирована способность целлюлозы длительно оставаться на слизистой носа и служить барьером для проникновения аллергенов, вместе с тем не только не нарушая функцию мукоциллиарного аппарата, но напротив, способствуя, в конечном итоге, ее восстановлению. Данный факт был показан в клиническом исследовании, проведенном у 100 детей и подростков с АР (в возрасте от 1,5 до 18 лет; средний возраст – 8,2 года). Уровень мукоцилиарного клиренса определялся in vivo с помощью метода простого не инвазивного нанесения контрастного вещества (3% Эдиколь Orange + СаНРО42Н20 97%). Измерение проводили дважды: до начала лечения и через 2 дня после завершения 6-недельного курса Назаваля. Выявлено увеличение скорости клиренса с 39 минут (средняя базальная скорость) до 18,15 минут после лечения (р<0.001). На начальном этапе исследования у 51 пациента был отмечен пролонгированный клиренс (средний показатель 55,23 мин при диапазоне от 31 до 80 мин). После лечения микродисперстным порошком целлюлозы этот показатель снизился до 21.1 мин. Только у 5 детей не было отмечено улучшений, скорость их мукоцилиарного клиренса осталась по-прежнему замедленной - более 37 мин.
Таким образом, в результате лечения Назавалем отмечено значительное улучшение в назальном мукоциллиарном клиренсе и скорости инспираторного потока (PNIFR), что обусловлено, по-видимому, регенерацией и нормализацией реснитчатого эпителия вследствие сокращения отека и аллергического воспаления.
Нарушение барьерных функций слизистых (их повышенная проницаемость) у больных аллергией является важнейшим звеном формирования аллергического ответа (8), что делает применение микродисперсной целлюлозы патогенетически обоснованным. В исследовании in vitro механизма действия геля, образуемого порошком микродисперсной инертной целлюлозы, показано, что диффузия аллергена клеща домашней пыли (Der р1) через гелеобразную пленку снижена значимо во все временные точки (15, 30, 45, 60, 180 и 360 минут). Через 15 мин только 0,76% от базального количества аллергена диффундировало через пленку; через 360 мин – 14% диффундировало, тогда как в контроле (агарный гель) диффузия аллергена была 100% (9). В другом клиническом исследовании продемонстрировано снижение эозинофильного катионного протеина (ЕСР) в назальном секрете пациентов, страдающих сезонным АР, которые до назальной провокации аллергена применяли порошок целлюлозы, что свидетельствует о превентивном в отношении аллергического воспаления действии Назаваля (10). После применения плацебо такого эффекта отмечено не было.
Клиническая эффективность Назаваля
Клиническая эффективность порошка микродисперсной целлюлозы продемонстрирована в нескольких зарубежных и отечественных исследованиях, проведенных у детей, подростков и взрослых, страдающих сезонным и круглогодичным АР. Большая часть этих исследований являются простыми, открытыми, наблюдательными, меньшая – двойными слепыми плацебо-контролируемыми исследованиями, но все они продемонстрировали эффективность применения микродисперсного порошка целлюлозы в профилактике и лечении АР.
В одном из первых исследований, проведенных в Англии на 102 взрослых больных сезонным АР, была показана эффективность Назаваля у 77% пациентов (11). После завершения 6-недельного периода исследования более 70% его участников оценили эффективность порошка целлюлозы как хорошую или высокую. Облегчение симптомов происходило в течение 0,1 – 3 часов после применения препарата. Побочные эффекты наблюдались редко, но на первой неделе 10% больных отметили, что легко вдыхают большой объем порошка и это вызывает неприятное ощущение в области задней стенки глотки. У одного пациента отмечался зуд в глазах, другой - отметил боль в горле. Однако эти симптомы могли быть также связаны с проявлениями АР. Трудности, возникшие при определении объема порошка, оставшегося во флаконе (из непрозрачного белого пластика), были наиболее распространенным неудобством, и в одном случае, когда порошок практически закончился, у участника немедленно возникли серьезные симптомы АР.
В двойном слепом плацебо-контролируемом исследовании две сравнимые группы пациентов принимали Назаваль или плацебо, а также другие препараты для лечения АР (12). В качестве критерия эффективности Назаваля было взято применение препаратов, необходимых для контроля симптомов. В исследование были включены 97 взрослых пациентов, имеющих симптомы АР в сезон пыления злаковых трав. Не было выявлено значимых различий в отношении симптомов АР в сравниваемых группах пациентов. Однако была выявлена существенная разница в объеме фармакотерапии, применяемой больными этих групп (Рис.3). Наиболее часто используемыми средствами были антигистаминные препараты. В активной группе 29% пациентов принимали только антигистаминные препараты, в сравнении с показателем группы плацебо (33%). Между группами не было отмечено значимых различий, однако при анализе применения антигистаминных средств в целом (т.е. количества больных, использующих антигистаминные препараты независимо от того, применялись ли они в качестве монотерапии или в сочетании с другими препаратами), соотношение пациентов в группе активного лечения составляло 34% в сравнении с группой плацебо - 48%, p < 0.05. Следующими по частоте использования были ИнГКС. С учетом всех дней с умеренным и выше уровнем содержания пыльцы травы в воздухе, 10% пациентов активной группы использовали назальные спреи в сравнении с 14% пациентов в группе плацебо (p < 0.05). 57% пациентов в активной группе принимали только инертный порошок целлюлозы и не использовали другие фармакологические препараты, в сравнении с 44% больных в группе плацебо (Рис.3). Результаты этого исследования свидетельствуют, что применение инертного порошка целлюлозы сокращает применение фармакологических лекарственных препаратов для контроля симптомов АР, что является особенно важным в некоторых популяциях больных: дети и пожилые люди, беременные и кормящие женщины.
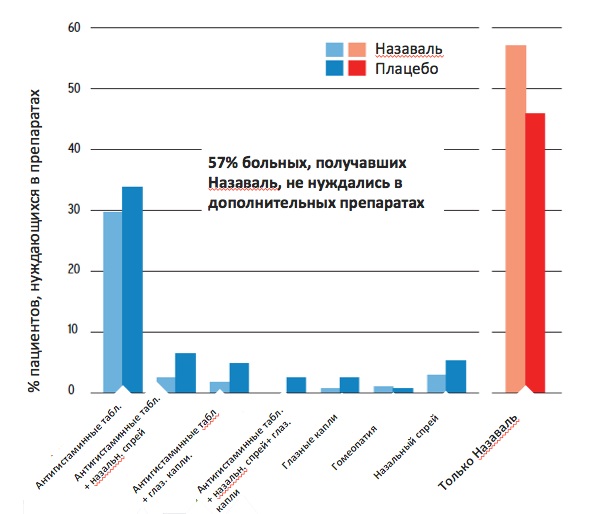
Рис.3 Пациенты (%), нуждающиеся в дополнительных препаратах, на фоне терапии Назавалем и плацебо (под назальным спреем авторы подразумевают ИнГКС) (12).
Превентивное применение Назаваля значимо улучшает назальное дыхание после провокации аллергеном, что было показано в двойном слепом плацебо-контролируемом исследовании Emberlin J и Lewis R (10). Разница в назальной пиковой скорости выдоха (ПСВ) после провокации аллергена луговых трав у больных, получавших микродисперсную целлюлозу, и пациентов, применявших плацебо, была достоверна во все временные точки после провокации (Рис.4). Эти же авторы провели аналогичное двойное слепое плацебо-контролируемое исследование с перекрестным дизайном у 15 пациентов с персистирующим АР, вызванным аллергией к клещу домашней пыли (13). Результаты продемонстрировали существенную разницу в выраженности симптомов АР (ринорея, чихание, зуд) (Рис.5) и уровне ЕСР в назальном секрете после назального провокационного теста с аллергеном клещей. Пациенты, получавшие Назаваль, имели значимо меньшую (р<0,05) интенсивность симптомов АР после провокации (Рис.5), что позволило авторам сделать вывод об эффективности порошка инертной целлюлозы в отношении редукции симптомов персистирующего АР, вызванного аллергией к клещу домашней пыли.
Отечественный опыт применения Назаваля
В РФ Назаваль зарегестрирован и разрешен к применению с 2009 года. Несколько отечественных исследований у взрослых и детей показали его эффективность в терапии АР.
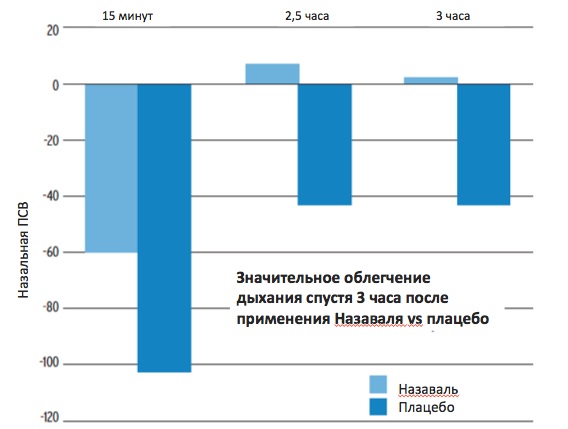
Рис.4 Разница между базальной назальной ПСВ и ПСВ после провокации специфическим аллергеном, р<0,01 во всех временных точках (ПСВ – пиковая скорость выдоха) (10).
Захаржевской Т.В. и коллегами (14) было проведено открытое не сравнительное исследование по оценке эффективности и безопасности спрея Назаваль в профилактике и лечении АР. В исследовании приняли участие 48 больных (25 взрослых и 23 детей) с АР. Длительность лечения составила 4 недели с еженедельной оценкой клинических проявлений АР. Было показано, что Назаваль уменьшает выраженность симптомов АР уже на первой неделе применения и улучшает качество жизни пациентов с АР более чем в 2 раза (Рис.6).
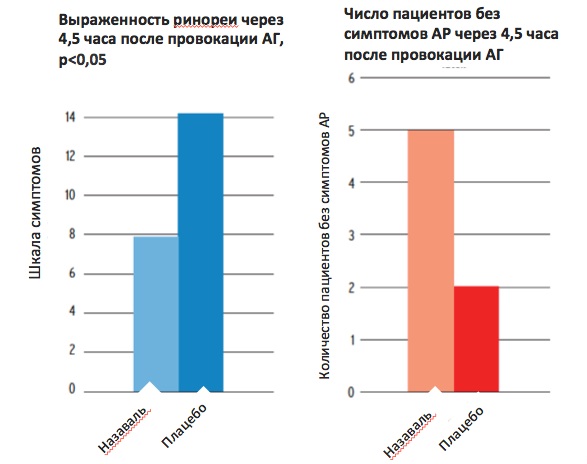
Рис.5 Разница в клинических проявлениях персистирующего АР после провокации аллергеном клеща домашней пыли у пациентов, применявших Назаваль и плацебо (13).
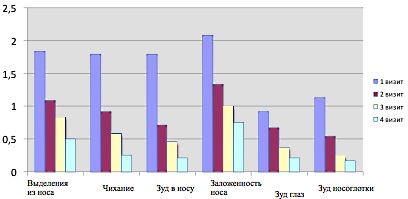
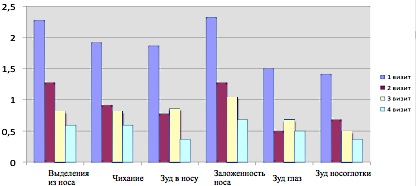
Рис.6 Динамика симптомов АР у детей (А) и у взрослых (Б) в результате 4-х недельного курса лечения Назавалем (степень тяжести АР: 0- симптомы отсутствуют; 1 - легкая (симптомы имеются, но не влияют на образ жизни); 2- умеренная (симптомы имеются, оказывают умеренное влияние на обычный образ жизни); 3- тяжелая (симптомы в выраженной степени ухудшают состояние и мешают заниматься повседневными делами) (14).
Н.А.Геппе с коллегами провели открытое сравнительное исследование эффективности и безопасности назального спрея Назаваль у 50 детей в возрасте от четырех до 14 лет с диагнозом сезонный АР (15). 30 детям был назначен препарат микродисперсного порошка целлюлозы, 20 детей вошли в группу сравнения и получали симптоматическую терапию. Оценивались объективные и субъективные симптомы сезонного АР до лечения и через 2, 4 и 6 недель после начала применения препарата. Симптомы оценивались по трехбальной шкале – 0 - отсутствие симптомов, 1 - слабая степень выраженности, 2- умеренная степень выраженности, 3- выраженные симптомы АР. В период наблюдения в обеих группах разрешено было использовать сосудосуживающие и антигистаминные препараты, назальные спреи ГКС за 15–20 минут до использования микродисперсного порошка целлюлозы. Через 2 недели от начала применения микродисперсного порошка целлюлозы Назаваль, в активной группе больных достоверно уменьшились все симптомы сезонного АР: ринорея - с 1,8±0,4 до 0,8±0,6 баллов; чихание – с 1,5±0,6 до 0,5±0,6; зуд в носу с 1,2±0,5 до 0,4±0,5; блокада носового дыхания с 1,8±0,5 до 0,7±0,6 (р<0,001) (Рис.7). У большинства пациентов (73%) отчетливое улучшение состояния отмечалось уже к пятому дню от начала применения Назаваля. В последующие 2 недели у 12 детей (40%) симптомы купировались полностью. У остальных детей отмечалось дальнейшее снижение симптомов АР.
Важным наблюдением этого исследования является влияние терапии Назавалем на сопутствующие АР симптомы конъюнктивита. Спустя две недели от начала лечения микродисперсным порошком инертной целлюлозы зуд глаз у пациентов уменьшился с 0,8±0,7 до 0,4±0,5 баллов, а через 4недели зуд глаз уменьшился до 0,2±0,3 баллов (Рис.7).
На фоне применения спрея Назаваль 9 детей (34,6%) получали эпизодически антигистаминные препараты, 7 детей (26,9%) – деконгестанты, 3-е детей (10%) – ИнГКС. В группе сравнения симптомы сохранялись на протяжении всего периода наблюдения, что требовало частого приема антигистаминных препаратов - 8 детей (40%), деконгестантов – 15 детей (75%), 8 пациентов (40%) использовали ИнГКС (Рис.8).
У 2-х детей (6,6%) со среднетяжелым сезонным АР препарат оказался малоэффективным и к терапии были добавлены ИнГКС. Двое детей (6,6%) отметили усиление чихания после применения препарата, им в дальнейшем Назаваль был отменен.
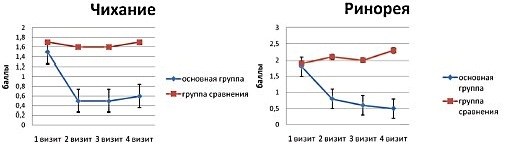
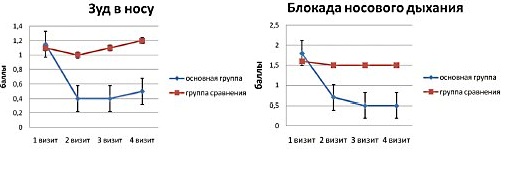
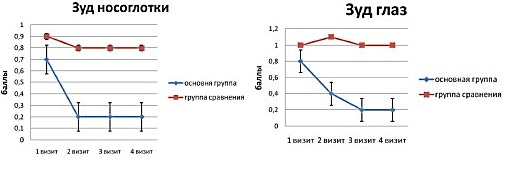
Рис.7 Динамика симптомов АР и конъюнктивита в результате терапии Назавалем и только фармакотерапии у детей с сезонным АР (15).
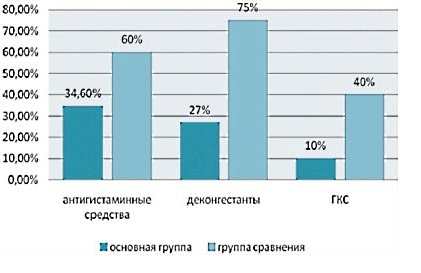
Рис.8 Частота применения фармакотерапии (% пациентов) в группах детей, получавших терапию Назавалем (основная группа) и группе сравнения (не получавших Назаваль) (15).
В целом большинство родителей и врачей (86,4%) оценили микродисперсный порошок целлюлозы как высокоэффективное средство для профилактики и лечения сезонного АР. Авторы делают заключение об эффективности микродисперсной целлюлозы для профилактики и лечения сезонного АР у детей, проявившейся не только в снижении интенсивности симптомов АР и сопутствующего конъюнктивита, но и потребности в дополнительной фармакотерапии.
В ФГБУ «ГНЦ Институт иммунологии» ФМБА России проведено открытое не сравнительное исследование по оценке эффективности препарата Назаваль у 30 взрослых пациентов, страдающих АР, вызванным пыльцевой аллергией (16). Оценка эффективности препарата проводилась на основании сравнения результатов провокационных назальных тестов, полученных до и после применения препарата Назаваль. Эффективность действия препарата Назаваль отмечена у 28 (99,6%) человек, что проявилось статистически достоверным уменьшением назальной реактивности на причинно-значимый аллерген. Средняя пороговая концентрация аллергена при проведении провокационных назальных тестов исходно составила 1250 PNU/мл, а после применения препарата Назаваль - 5000 PNU/мл (p<0,001), при этом 4 пациента не отметили развитие симптомов даже при провокации максимальной концентрации аллергена 10000 PNU/мл. Лучшие результаты были получены у пациентов с изолированной пыльцевой сенсибилизацией и легким течением ринита. Двое пациентов, у которых не отмечено эффективности препарата, имели сочетанную пыльцевую и бытовую сенсибилизацию. Авторами высказывается предположение, что наличие бытовой сенсибилизации обуславливает персистирующее аллергическое воспаление слизистой носа и повышенную назальную гиперреактивость, даже в отсутствии клинических проявлений ринита. Поскольку Назаваль не обладает противовоспалительным или противоаллергическим действием, нельзя ожидать, что препарат сможет повлиять на течение уже развившейся аллергической реакции, но в составе комплексной терапии АР препарат сможет блокировать дальнейшее поступление аллергена с вдыхаемым воздухом. В этом исследовании ни у одного из пациентов не отмечено ни одного нежелательного явления.
Заключение
Таким образом, порошок микродисперсной инертной целлюлозы (Назаваль) является эффективным средством профилактики развития симптомов аллергического ринита: зуда в носу, отека слизистой носа и нарушения носового дыхания, обильных слизистых выделений из носа, приступов чихания и зуда глаз. Применение препарата будет более эффективным, если начинать его использование до начала и продолжать в течение всего периода контакта с аллергеном. Вместе с тем Назаваль уменьшает выраженность уже развившихся симптомов АР у взрослых и детей и способствует сокращению объема фармакотерапии.
Важным преимуществом Назаваля является его безопасность и возможность использования у детей и пожилых лиц, женщин в период беременности и кормления грудью, так как он не содержит действующих фармакологических веществ и не обладает системным действием.
Литература:
1. Bousquet J., N. Khaltaev, A. Cruz et al. Allergic Rhinitis and its Impact on Asthma (ARIA) 2008 Update //Allergy. – 2008. – Vol. 63. (Suppl.86) – p.1-160
2. Ozdoganoglu T, Songu M. The Burden of Allergic Rhinitis and Asthma. Ther Adv Resp Dis. 2012;6(1):11-23
3. Богова А.В., Ильина Н.И., Лусс Л.В. Тенденции в изучении эпидемиологии аллергических заболеваний в России за последние 10 лет. Российский аллергологический журнал. 2008;6:3-14
4. Ненашева Н.М., Буриев Б.Б. Особенности атопической бронхиальной астмы у взрослых. Российский аллергологический журнал.- 2009.- №4, С.12-17
5. Bousquet J, Anto JM. Demoly P, et al. Severe Chronic Allergic (and Related) Diseases: A Uniform Approach – A MeDALL – GA 2 LEN –ARIA Position Paper. Int Arch Allergy Immunol 2012;158:216–231
6. Bousquet J, Lund VJ, Van Cauwenberge P, et al: Implementation of guidelines for seasonal allergic rhinitis: a randomized controlled trial. Allergy 2003; 58: 733–741
7. Diethart B, Emberlin J, Lewis R. Nasal mucociliary clearance and mucoadhesion of hydroxypropylmethylcellulose powder used for alleviation of allergic rhinitis. Pediatric Allergy and Immunology 22 (2011) 594–599
8. Holgate St.T. Epithelium dysfunction in asthma. J.Allergy Clin. Immunol. 2007, v.120, p.1233-1244
9. Diethart B, Emberlin J, Lewis R. Nasaleze cellulose powder delays house dust mite allergen (Der p1) diffusion in vitro. Natural Science Vol.2, No.2, 79-84 (2010)
10. Emberlin JC, Lewis RA. Efficacy of Nasaleze for use in hayfever via pollen provocation tests. Presented as a Poster at EAACI, Vienna June 2006; p370
11. Josling P, Steadman S. Use of cellulose powder for the treatment of seasonal allergic rhinitis Adv Ther. 2003;20(4):213-9
12. Emberlin JC, Lewis RA. Double blind placebo controlled cross over trial of inert cellulose powder, by nasal provocation with grass pollen to assess efficacy of the product in controlling symptoms of hay ferer. Curr Med Res Opin, 2006; 22(2):275-285
13. Emberlin J, Lewis R. Double blind placebo controlled cross-over trial of Nasaleze by nasal provocation tests with Der p1 and Der f1. Curr Med Res Opin 2007:23(10): 22423-2431
14. Захаржевская Т. В., Сидоренко И. В., Трескунов В. К., Караулов А. В. Возможности использования нового назального спрея Назаваль в лечении и профилактике аллергического ринита. Российский аллергологический журнал, 2009, № 4, с. 82–86
15. Геппе Н. А., Снегоцкая М. Н., Конопелько О.Ю. Новое в профилактике и терапии сезонных аллергических ринитов у детей. Лечащий врач. 2010;1: С.39-43
16. Ильина Н.И., Курбачева О.М., Микеладзе К.Р., Павлова К.С., Швец С.М. Лечебное и профилактическое действие назального спрея Назаваль у больных аллергическим ринитом. Обзор зарубежных и отечественных клинических исследований. Российский аллергологический журнал, 2011,2:78-85
17. Allergies in America. A telephone survey conducted in 2500 adults with allergic rhinitis. Healthstar Communications, Inc., in partnership with Shulman, Ronca and Bucuvalas, Inc. Allergies in America: A landmark survey on nasal allergy sufferers. Executive summary. Florham Park, NJ: Altana Pharma US, Inc., 2006
- Войдите или зарегистрируйтесь, чтобы получить возможность отправлять комментарии