| Новости | e-Образование | Врачебные Общества | Тематические группы | Библиотека | Медиатека | Мероприятия | Атлас |
Присоединяйтесь!
- Повышение квалификации
- Сертифицированное образование
- Актуальные статьи
- Обзоры и репортажи
- Клинические случаи
- Новости медицины
- Советы коллег
Сообщество: Оценка Медицинских Технологий
Клинико-экономическая оценка использования сугаммадекса (Брайдана) для реверсии нейромышечного блока при проведении оперативных
Клинико-экономическая оценка использования сугаммадекса (Брайдана) для реверсии нейромышечного блока при проведении оперативных вмешательств
Е.В. Деркач1, М.В. Авксентьева2, 3, О.Ю. Реброва1, 4, Е.М. Шифман5, В.И. Игнатьева1, 2, 3, Э.М. Николаенко6
1. Автономная некоммерческая организация «Национальный центр по оценке технологий в здравоохранении», Москва, Россия
2. Центр по оценке технологий в здравоохранении Института прикладных экономических исследований Российской академии народного хозяйства и государственной службы при Президенте РФ, Москва, Россия
4. Российский национальный исследовательский медицинский университет им. Н.И. Пирогова Минздрава РФ, Москва, Россия
5. Научный центр акушерства, гинекологии и перинатологии им. академика В.И. Кулакова Минздрава РФ, Москва, Россия
6. Центр анестезиологии и интенсивной терапии Центральной клинической больницы №1 открытого акционерного общества «Российские железные дороги», Москва, Россия
Цель. Провести клинико-экономический анализ использования сугаммадекса для реверсии НМБ, вызванного рокурония бромидом, при проведении оперативных вмешательств под общей анестезией с искусственной вентиляцией легких (ИВЛ) по сравнению с альтернативной тактикой: реверсией НМБ без использования сугаммадекса, при этом в 38% случаев выполняется реверсия НМБ с использованием неостигмина, а в остальных случаях происходит спонтанная реверсия НМБ.
Методы. На основе результатов клинических исследований, данных маркетингового исследования практики проведения анестезии в РФ и опроса экспертов-анестезиологов на базе программного обеспечения Microsoft Excel построена модель для оценки влияния использования сугаммадекса для реверсии НМБ на бюджет стационара. Модель учитывает затраты на медикаментозное обеспечение реверсии НМБ (сугаммадексом или неостигмином), затраты на кислород для обеспечения ИВЛ в период восстановления нейромышечной проводимости, а также расходы, связанные с дополнительными (незапланированными) случаями перевода больных в отделения реанимации и интенсивной терапии (ОРИТ) при необходимости лечения осложнений. На заключительном этапе в модели рассчитывается потенциальный доход стационара: увеличение объема финансирования за оказанную медицинскую помощь (в соответствии с нормативами финансовых затрат в системе здравоохранения РФ) благодаря большему числу пролеченных больных, в зависимости от вида операций, которые можно выполнить в освободившееся время. Результаты. Моделирование на примере стационара, выполняющего за год 5000 операций, из них 160 - под общей анестезией с ИВЛ с использованием рокурония, показало, что при рациональном управлении работой операционных не только окупаются затраты на применение при этих вмешательствах сугаммадекса (881 938 руб. в год), но и ожидается за счет увеличения числа проведенных операций получение дополнительного финансирования на оказание медицинской помощи в размере от 619 тыс. до 2 млн руб. в год (в зависимости от вида оперативных вмешательств, которые будут выполняться в освободившееся время).
Заключение. Применение сугаммадекса для реверсии НМБ, вызванного рокурония бромидом, является экономически целесообразным, так как позволяет уменьшить частоту случаев развития остаточного НМБ и ассоциированных с ним осложнений, сократить время занятости операционной в расчете на одну операцию и высвободить время для выполнения дополнительных операций. При рациональном планировании работы операционного блока это должно привести: с позиции системы здравоохранения - к повышению доступности медицинской помощи, а с позиции стационара - к увеличению объема финансирования.
Обязательным компонентом общей анестезии с искусственной вентиляцией легких (ИВЛ) является нейромышечный блок (НМБ), который достигается путем применения миорелаксантов - препаратов, блокирующих нейромышечную проводимость (НМП). В настоящее время на фармацевтическом рынке имеется достаточно широкий ассортимент миорелаксантов, различающихся по времени наступления эффекта, равномерности распределения препарата в мышечной ткани, глубине НМБ и длительности действия. Выбор препарата в каждом конкретном случае определяется как объективными характеристиками пациента и предстоящего оперативного вмешательства, так и предпочтениями анестезиолога. Однако все миорелаксанты обладают рядом побочных эффектов, одним из которых является остаточная кураризация, или остаточный НМБ - продолжающееся после окончания оперативного вмешательства действие миорелаксантов, которое приводит к нарушениям дыхания, защитных дыхательных рефлексов, глотания и вызывает кашель.
Возможная связь между остаточным НМБ и риском осложнений после анестезии была показана в ряде исследований [1-6]. По мнению многих экспертов, значимость остаточного НМБ и частота осложнений на его фоне недооцениваются анестезиологами в реальной практике [7-9]. По разным данным, при отсутствии объективного мониторинга по окончании оперативного вмешательства и анестезии анестезиолог-реаниматолог в 45-60% случаев экстубирует пациента, пребывающего в состоянии остаточного НМБ, что повышает риск развития послеоперационной гипоксии и гиповентиляции [10]. Актуальность проблемы остаточного НМБ для отечественной анестезиологии обсуждается в ряде публикаций [11-16]; часть из них представляет собой обзоры зарубежных исследований, но есть, пусть и ограниченные, локальные данные. О признании важности проблемы остаточного НМБ свидетельствует, например, наличие рекомендаций по диагностике и реверсии остаточного НМБ в нейрохирургии, разработанных «Обществом нейроанестезиологов и нейрореаниматологов» [11].
В ряде случаев анестезиологи для реверсии НМБ используют антагонисты курареподобных средств; для антидеполяризующих средств это антихолинэстеразные средства (неостигмин). Однако, судя по недавно выполненным клиническим исследованиям, эффективность неостигмина сомнительна, реверсия НМБ при помощи ингибиторов ацетилхолинэстеразы зачастую сопровождается неполным восстановлением НМП и высоким риском рекураризации, что, в свою очередь, повышает риск послеоперационных респираторных осложнений [12, 17]. Также существенным недостатком использования ингибиторов ацетилхолинэстеразы является высокая частота развития побочных М-холинергических эффектов (брадикардия, вплоть до остановки сердца, бронхоспазм, усиление секреции бронхиальных желез, генерализованная реакция электроэнцелографической активации, усиление перистальтики пищевода, желудка, кишечника, повышение секреции пищеварительных желез).
Сугаммадекс (Брайдан®) предназначен для реверсии НМБ, вызванного рокуронием. Как показали рандомизированные клинические исследования (РКИ) и систематические обзоры РКИ, использование сугаммадекса обеспечивает более быструю и предсказуемую реверсию НМБ по сравнению со спонтанной реверсией и неостигмином [18, 19]. Было также продемонстрировано, что применение сугаммадекса снижает частоту остаточного НМБ в момент восстановления после анестезии [18], что позволяет предполагать и снижение риска связанных с ним осложнений.
Экономическая целесообразность применения сугаммадекса изучалась в значительном количестве зарубежных исследований [19-30]. Большая часть из них основана на гипотезе о возможности более рационального использования операционных и/или послеоперационных палат за счет сокращения времени восстановления НМП: быстрая реверсия НМБ позволяет сократить период пребывания больного в операционной или в послеоперационной палате, а высвободившееся время можно использовать для проведения дополнительных операций. Однако до сих пор нет посвященных этой проблеме отечественных работ, что и послужило предпосылкой для проведения настоящего исследования.
Целью исследования являлось выполнение клинико-экономического анализа использования сугаммадекса для реверсии НМБ, вызванного рокурония бромидом, при проведении оперативных вмешательств под общей анестезией с ИВЛ.
Для достижения указанной цели были поставлены следующие задачи:
- Анализ литературных данных о частоте остаточного НМБ в клинической практике и риске развития ассоциированных с ним осложнений.
- Поиск и анализ доказательств эффективности и безопасности сугаммадекса для реверсии НМБ.
- Построение модели для оценки влияния использования сугаммадекса для реверсии НМБ на бюджет стационара.
- Определение затрат стационара на использование сугаммадекса для реверсии НМБ, вызванного рокурония бромидом, и прогнозирование повышения оперативной активности благодаря сокращению времени занятости операционной в расчете на одну операцию.
Методика исследования
Гипотеза исследования и ее обоснование
Гипотеза исследования заключалась в следующем: использование сугаммадекса для реверсии НМБ, вызванного рокурония бромидом при операциях под общей анестезией с ИВЛ, позволит уменьшить частоту случаев развития остаточного НМБ и ассоциированных с ним осложнений, сократить время занятости операционной в расчете на одну операцию и высвободить время для выполнения дополнительных операций, что при рациональном планировании работы операционного блока должно привести к повышению доступности медицинской помощи и увеличению объема финансирования (дохода) медицинской организации.
Обоснованием гипотезы исследования послужили результаты РКИ, изучавших частоту развития остаточного НМБ и время до начала экстубации больного при использовании сугаммадекса.
Разница в частоте остаточного НМБ, устанавливаемого при значении критерия TOF(train-of-fourstimulation- серия из четырех) <0,9, во время экстубации трахеи после реверсии индуцированного рокуронием глубокого НМБ сугаммадексом 4,0 мг/кг и нео-стигмином 50 мг/кг (в комбинации с гликопирролатом в дозе 10 мг/кг) изучалась в РКИ SaboD. etal., 2011 [31]. Отношение TOF>0,9 во время или перед экстубацией было достигнуто в 96,0% случаев использования сугаммадекса и лишь в 39,5% случаев использования неостигмина (Р<0,0001). Также существуют данные квазиэкспериментального исследования о том, что применение использующихся в типичной практике препаратов для реверсии НМБ не дает статистически значимого снижения частоты остаточного НМБ [32].
В исследовании группы пациентов с сердечно-сосудистой патологией, которым проводились различные общехирургические вмешательства, время восстановления индуцированного рокуронием НМБ от начала введения препарата до достижения TOF>0,9 составило в среднем 1,7 мин при использовании сугаммадекса (2,0 мг/кг) против 34,3 мин в группе плацебо [33]. В другом исследовании учитывалось среднее общее время, проведенное больным в операционной (с учетом длительности хирургического вмешательства - лапароскопической холецистэктомии) при применении сугаммадекса и неостгмина, оно составило 64,4 мин (от 51,9 до 76,9 мин) и 80,3 мин (от 69,8 до 90,8 мин) соответственно (Р<0,05) [21].
В ряде клинических исследований различного дизайна изучались негативные последствия остаточного НМБ. Было обнаружено, что остаточный НМБ у здоровых добровольцев приводит к нарушениям функций глотания и дыхания, что свидетельствует о потенциальном повышении риска развития осложнений у больных, перенесших оперативные вмешательства [1-3, 6]. Выявлена связь между остаточным НМБ и развитием гипоксемии и другими критическими нарушениями дыхания; общая частота таких событий в популяции прооперированных больных может составлять около 1% [4]. Косвенным свидетельством негативного влияния остаточного НМБ на состояние здоровья является то, что в стационарах, где экстубация пациента проводится в послеоперационной палате, длительность пребывания в этом подразделении статистически значимо выше у пациентов с остаточным НМБ, чем у пациентов с полной реверсией [34].
Построение клинико-экономической модели
В модели на базе MSExcelпроведен анализ влияния на бюджет стационара технологии реверсии НМБ, индуцированного рокурония бромидом, при помощи препарата сугаммадекс у больных, перенесших оперативное вмешательство под общей анестезией.
Начальной точкой модели является совокупность всех хирургических вмешательств в гипотетическом стационаре, где выполняется 5000 операций в год. Исходя из данных о долях операций, проводимых под общей анестезией с ИВЛ с применением стероидных деполяризующих миорелаксантов и конкретно рокурония, определено число операций, где потенциально может применяться сугаммадекс для реверсии НМБ, т. е. операций под общей анестезией с ИВЛ, проводимой с применением рокурония в качестве миорелаксанта.
Далее в модели прогнозируется развитие остаточного НМБ в гипотетической когорте больных в двух альтернативных сценариях:
- 1-й сценарий (текущая практика) - восстановление НМП после блока, вызванного рокуронием, происходит без использования сугаммадекса, при этом в 38% случаев выполняется реверсия НМБ с использованием неостигмина, а в остальных случаях происходит спонтанная реверсия НМБ;
- 2-й сценарий - в 100% случаев операций, проводимых с применением рокурония, для реверсии НМБ используется сугаммадекс.
В модели определены:
- дополнительные затраты медицинской организации на применение сугаммадекса у всех больных, перенесших оперативное вмешательство под общей анестезией с применением рокурония;
- потенциальная экономия расходов медицинской организации, обусловленная уменьшением времени выхода из НМБ и снижением числа осложнений, ассоциированных с остаточным НМБ;
- время занятости операционных, которое экономится благодаря более раннему восстановлению НМП и быстрой экстубации пациента. Экономия средств за счет уменьшения времени выхода из НМБ и снижения числа осложнений, ассоциированных с остаточным НМБ, складывается из расходов на кислород, который получает больной до момента экстубации, и расходов, связанных с дополнительными (незапланированными) случаями перевода больных в ОРИТ при необходимости лечения возможных осложнений остаточного НМБ.
Разница между временем занятости операционной в период восстановления НМП (от момента завершения операции до экстубации) при использовании неостигмина или при спонтанной реверсии - и временем до экстубации при применении сугаммадекса - расценивается как упущенная возможность дополнительных случаев лечения: иными словами, как время, которое можно было бы использовать для проведения дополнительных оперативных вмешательств. В модели прогнозируется, какой потенциальный доход может получить стационар благодаря увеличению объема финансирования за оказанную медицинскую помощь большему числу пролеченных больных.
Результаты моделирования представлены в виде суммы (в рублях), которую необходимо вложить дополнительно (или можно сэкономить) при внедрении в широкую практику использования сугаммадекса для реверсии НМБ, вызванного рокуронием, т.е. при замене первого сценария ведения больных в данной модели на второй.
Основные условия модели:
- экстубация больного проводится в операционной;
- после операции часть больных планово поступает в ОРИТ, остальные после пробуждения переводятся в профильное отделение и поступают в ОРИТ только в случае развития осложнений, обусловливающих необходимость реанимационной помощи или интенсивной терапии;
- в стационаре осуществляется рациональное планирование работы операционного блока, позволяющее проводить дополнительные операции в высвободившееся время;
- оплата оказания стационарной медицинской помощи производится по законченному случаю, и стационар заинтересован в увеличении числа оперативных вмешательств и госпитализаций.
Входные параметры модели
Значения входных частотных параметров модели были определены на основе анализа результатов следующих работ:
- РКИ сугаммадекса, оценивающих его эффективность в сравнении с плацебо и неостигмином;
- исследований частоты развития НМБ и его осложнений;
- маркетингового исследования, изучавшего типичную анестезиологическую практику в РФ (на основе опроса 515 врачей-анестезиологов из 14 городов РФ, работающих в составе хирургических бригад не реже 10 раз в неделю, с опытом работы от 2 до 30 лет);
- дополнительно проведенного в ходе настоящего исследования опроса 10 врачей-анестезиологов. Значения входных параметров и источники информации о них приведены в табл. 1.
Значения стоимостных показателей и источники информации о них приведены в табл. 2. Расчет затрат проводился с позиции медицинской организации. Затраты на лекарственные препараты рассчитаны на основе цен заключенных контрактов на приобретение лекарств и зарегистрированных предельных отпускных цен производителей на лекарственные препараты, включенные в Перечень ЖНВЛП. Расходы на кислород рассчитаны на основе оптовых цен. Для расчета затрат на пребывание больного в ОРИТ использованы тарифы ОМС г. Москвы с поправочным коэффициентом, отражающим долю средств ОМС в общих расходах здравоохранения7.
Таблица 1. Входные параметры модели
| Показатель | Значение показателя | Источник данных |
|---|---|---|
| Частота общей анестезии при проведении оперативных вмешательств, % |
70,88 |
Маркетинговое исследование* |
| Частота использования ИВЛ, % |
68,00 |
|
| Частота использования эндотрахеальной анестезии, % |
85,70 |
|
| Частота использования стероидных недеполяризующих миорелаксантов, % |
64,00 |
|
| Частота использования рокурония, % |
12,10 |
|
| Частота реверсии НМБ неостигмином в реальной практике, % |
38,20 |
|
| Частота планового перевода больных в ОРИТ после операции, % |
20,00 |
Опрос экспертов |
| Частота внеплановых переводов в ОРИТ по поводу осложнений остаточного НМБ, % |
0,01 |
Haller G. et al., 2005 [35], Haller G. et al., 2008 [36], Piercy M. et al., 2006 [37], Eichenberger A. et al., 2011 [38] |
| Частота остаточного НМБ, % |
|
|
| при реверсии НМБ неостигмином или без него |
60,47 |
Sabo D. et al.,2011 [31] |
| при реверсии НМБ сугаммадексом |
4,00 |
Sabo D. et al.,2011 [31] |
| Экономия времени занятости операционной, мин |
|
|
| сугаммадекс по сравнению со спонтанной реверсией НМБ |
33 |
Dahl V. et al.,2009 [33] |
| сугаммадекс по сравнению с неостигмином |
16 |
Grintescu I. et al.,2009 [21] |
* Маркетинговое исследование мнений анестезиологов по вопросам общей анестезии, «TopofMind», Москва, 2007 (неопубликованные данные).
Таблица 2. Стоимостные показатели модели
| Показатель | Значение показателя, руб. | Источник данных |
|---|---|---|
| Цена препаратов в расчете на одно хирургическое вмешательство |
|
|
| неостигмин 2 мг + атропина сульфат 1,5 мг* |
7 |
www.grls.rosminzdrav.ru |
| сугаммадекс** |
6742 |
www.zakupki.gov.ru;
закупки с 21.03.2011 по 07.03.2013
|
| Цена кислорода, расходуемого за одну минуту*** |
45 |
www.kislorod.net |
| Стоимость одних суток пребывания в ОРИТ**** |
7513 |
Тарифы ОМС г. Москвы на 2011 г. |
* Согласно инструкции по применению препарата неостигмин, для купирования действия миорелаксантов вводят 1,5 мг препарата после предварительного введения 0,5-0,7 мг атропина сульфата; при необходимости инъекции повторяют в общей дозе не более 5-6 мг в течение 20-30 мин; установленная суточная доза (DefinedDailyDose, DDD) неостигмина для применения по основному показанию у взрослых равна 2 мг парентерально.
" Исходя из количества препарата, необходимого для реверсии управляемого НМБ (2 мг/кг), на 1 пациента весом 70 кг требуется 140 мг препарата; в расчетах учтена цена полного флакона, содержащего 200 мг препарата. Сугаммадекс не входит в Перечень ЖНВЛП, поэтому для расчетов использована средняя цена государственных контрактов.
"* Исходя из скорости введения 100% кислорода 5 л/мин [39].
"** Исходя из возмещения расходов в г. Москве по КСГ «Реанимация 1-й категории сложности» 8078 руб. за два койко-дня [40]. С учетом требований нормативных документов [40] было принято допущение, что в случае перевода больного в ОРИТ по поводу развития остаточного НМБ более чем на 6 часов, длительность пребывания ограничивается одним койко-днем.
В модели предполагается использование высвободившегося времени работы операционных для проведения оперативных вмешательств, имеющих среднюю продолжительность в пределах одного часа. При этом выгода для стационара состоит в возможности получения дополнительного финансирования за каждый дополнительный случай госпитализации по поводу основного заболевания, являющегося показанием к хирургическому вмешательству. Перечень хирургических операций, которые можно провести в освободившееся в работе операционной время, и стоимость законченного случая госпитализации, соответствующего каждой операции (по тарифам ОМС г. Москвы), приведены в табл. 3. Все выбранные нами для этой части модели операции, по нашему предположению, требуют использования рокурония, а, следовательно, и последующего применения сугаммадекса. Поэтому из суммы дополнительного финансирования, которое может получить стационар в случае альтернативных вариантов использования освободившегося времени, были исключены затраты на сугаммадекс в количестве, необходимом для выполнения этих операций.
Таблица 3. Стоимость дополнительных случаев оперативного лечения
| Название медицинского стандарта по клинико-статистической группе | Название операции | ВСЕГО на случай лечения*, руб. |
|---|---|---|
| Полипы носа, кисты носового синуса. Хронический синусит (дети) |
Полипотомия носа с этмоидотомией |
41 205 |
| Хронический калькулезный холецистит неосложненный |
Холецистэктомия при хроническом холецистите |
43 291 |
| Хронический калькулезный холецистит неосложненный |
Эндохирургическая холецистэктомия |
48 879 |
| Грыжи передней брюшной стенки неосложненные |
Грыжесечение при грыжах белой линии живота |
31 576 |
| Доброкачественные образования матки |
Консервативная миомэктомия |
38 447 |
| Варикозное расширение вен нижних конечностей без осложнений |
Иссечение варикозно расширенных вен (комбинированная флебэктомия) |
28 195 |
| Аденома предстательной железы |
Аденомэктомия |
43 536 |
* Стоимость случая складывается из тарифа на оперативное вмешательство, анестезиологическое пособие и законченный случай пребывания в стационаре; использовались тарифы ОМС г. Москвы [40] с поправочным коэффициентом 1,86.
Проведен анализ чувствительности результатов расчетов к колебаниям значения стоимости законченного случая лечения хирургического больного. Возможный разброс значений стоимости законченного случая был принят равным разбросу показателя фактического финансирования одного койко-дня в субъектах Российской Федерации по сведениям из доклада о реализации Программы государственных гарантий в 2011 г. (в процентах от исходного значения, использованного в модели) [42]. Также выполнен анализ чувствительности к колебаниям частоты применения рокурония бромида, а именно к ее повышению с 12% (частота, принятая в базовой модели) до 25%.
Результаты
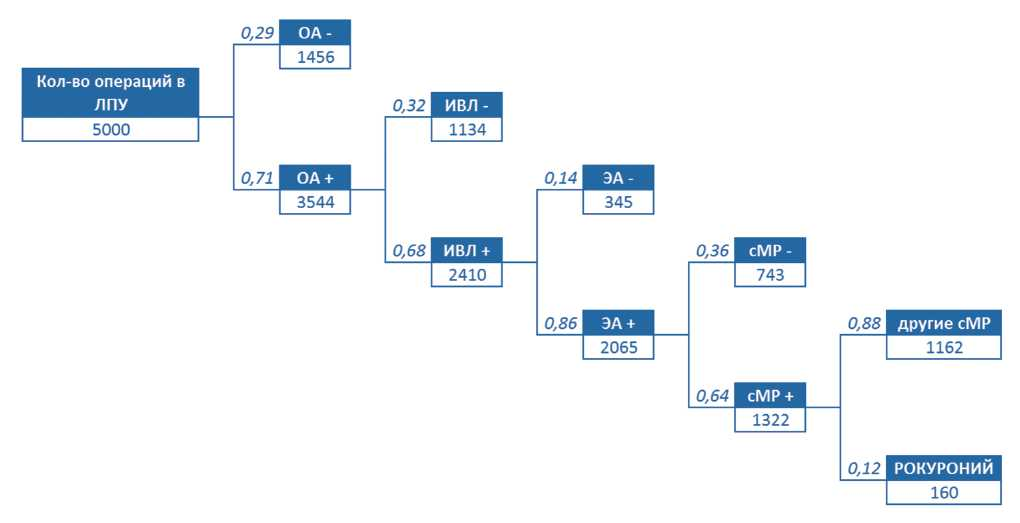
В стационаре, выполняющем 5000 хирургических операций в год, с учетом параметров, заложенных в модель (см. табл. 1), может выполняться 160 операций под общей анестезией с ИВЛ с использованием рокурония (рис. 1).
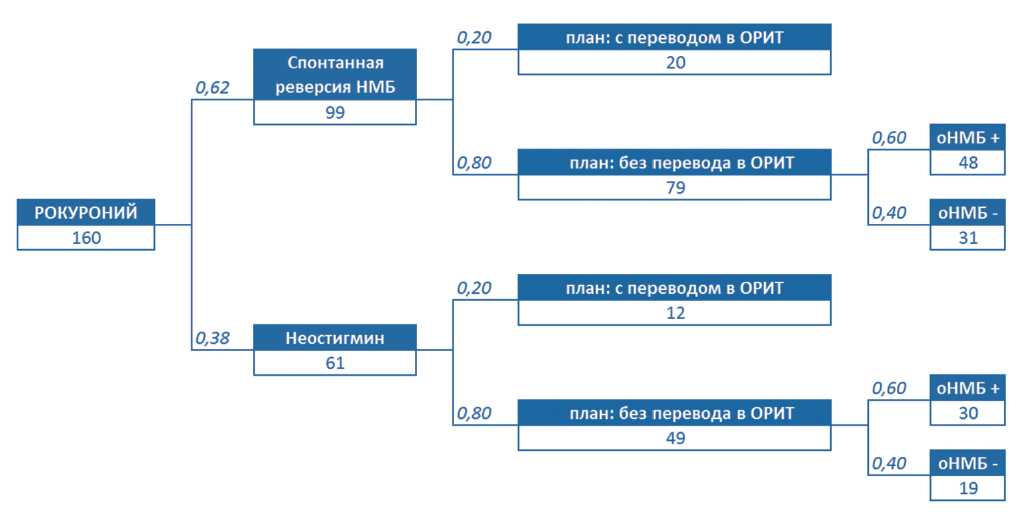
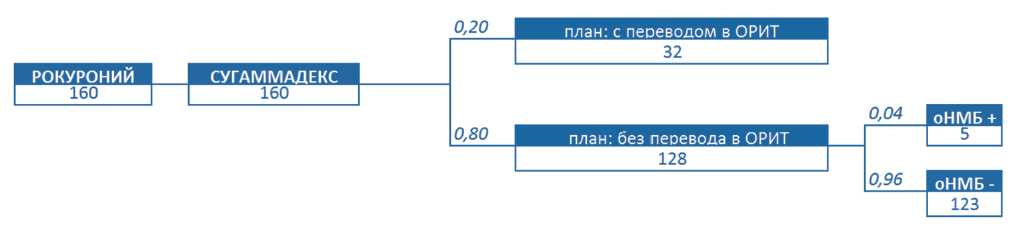
При ведении больных без использования сугаммадекса может прогнозироваться развитие остаточного НМБ в 78 случаях, в том числе в 48 случаях после спонтанной реверсии НМБ и в 30 случаях после применения неостигмина (рис. 2). При альтернативном подходе к восстановлению НМП, включающем использование сугаммадекса во всех случаях индукции НМБ рокуронием, остаточный НМБ можно ожидать только у 5 больных из 160 (рис. 3). Таким образом, внедрение реверсии НМБ с применением сугаммадекса, согласно приведенной модели, позволит стационару сократить число случаев остаточного НМБ в 15 раз (с 78 до 5 случаев в год). С учетом принятого в настоящем исследовании предположения, что 1,0% осложнений остаточного НМБ требует перевода больных в ОРИТ, использование сугаммадекса позволит предупредить один случай перевода в ОРИТ в течение года.
Рис. 1. Моделирование числа операций под общей анестезией с ИВЛ с использованием рокурония.
Примечания:
ОА - общая анестезия; ИВЛ - искусственная вентиляция легких; ЭА - эндотрахеальная анестезия;
сМР - использование стероидных недеполяризующих мышечных релаксантов; +/- проводится / не проводится
Рис. 2. Моделирование процесса восстановления НМП до внедрения использования сугаммадекса.
Примечание:
оНМБ - остаточный нейромышечный блок
Рис. 3. Моделирование процесса восстановления НМП после использования сугаммадекса.
Примечание:
оНМБ - остаточный нейромышечный блок
Экономия времени занятости операционной благодаря сокращению периода восстановления НМП может составить 70 часов, в том числе:
- 54 часа освобождается за счет использования сугаммадекса вместо спонтанной реверсии НМБ у 99 больных (экономия 33 мин на каждый случай);
- 16 часов - за счет использования сугаммадекса вместо неостигмина у 61 больного (экономия 16 мин на каждый случай).
В целом, внедрение в практику работы медицинской организации использования сугаммадекса оказывает следующее влияние на бюджет:
- исключаются расходы на использование неостигмина (с атропином) у 61 больного в размере 410 руб. в год;
- исключаются расходы на кислород для обеспечения ИВЛ в период восстановления НМП в размере 188 879 руб. в год;
- исключаются расходы на оказание медицинской помощи в ОРИТ, связанное с развитием осложнений остаточного НМБ, в размере 7513 руб. в год;
- добавляются расходы на препарат сугаммадекс (в количестве, необходимом для обеспечения реверсии НМБ всем больным, получавшим рокуроний) в размере 1 078 739 руб. в год.
Таким образом, совокупное влияние на бюджет ЛПУ в результате изменения потребления ресурсов выражается в необходимости дополнительного финансирования в размере 881 938 руб. в год (табл. 4).
Время занятости операционных, освободившееся в результате использования сугаммадекса, может быть использовано в стационаре как возможность получения финансирования за проведение дополнительных операций. В табл. 5 представлены результаты расчета потенциального объема дополнительного финансирования больницы при проведении разных вариантов оперативных вмешательств в высвободившееся время. Наиболее перспективным может быть внедрение данной технологии в учреждениях с большим потоком операций эндохирургической холецистэктомии.
Таблица 4. Изменение потребления ресурсов в модели до и после внедрения использования сугаммадекса
| Экономические ресурсы | До внедрения сугаммадекса | После внедрения сугаммадекса | Влияние на бюджет |
|---|---|---|---|
| Стоимость медикаментозного обеспечения реверсии НМБ |
410 |
1 078 739 |
-1 078 329 |
| Стоимость кислорода для обеспечения ИВЛ в период восстановления НМП |
188 879 |
- |
188 879 |
| Стоимость внепланового перевода ОРИТ в связи с осложнениями оНМБ |
7513 |
- |
7513 |
| ИТОГО |
196 801 |
1 078 739 |
- 881 938 |
Таблица 5. Увеличение финансирования медицинской организации при различных вариантах использования освободившегося времени операционных (базовая модель)
| Дополнительный случай лечения | Размер дополнительного финансирования, руб.* | Увеличение финансирования стационара, руб. |
|---|---|---|
| Холецистэктомия |
2 556 746 |
1 674 807 |
| Эндохирургическая холецистэктомия |
2 947 715 |
2 065 777 |
| Операция по поводу полипов носа |
2 410 816 |
1 528 878 |
| Операция по поводу неосложненной грыжи передней брюшной стенки |
1 737 222 |
855 284 |
| Операция по поводу доброкачественного новообразования матки |
2 217 907 |
1 335 969 |
| Операция по поводу варикозного расширения вен |
1 500 718 |
618 780 |
| Операция по поводу аденомы предстательной железы |
2 573 936 |
1 691 998 |
* Объем возмещения расходов в расчете на 70 дополнительных случаев госпитализации с проведением оперативного вмешательства за вычетом расходов на сугаммадекс.
Анализ чувствительности
Результаты анализа чувствительности показали, что даже при снижении объема возмещения расходов на отдельный случай лечения хирургического больного медицинская организация может благодаря внедрению сугаммадекса получить дополнительный объем финансирования за счет проведения определенных видов оперативных вмешательств в высвободившееся время (табл. 6). Так, если норматив финансирования за каждый случай составляет всего 29% от исходного (такая ситуация, судя по соотношению финансирования койко-дня, характерна для 25% субъектов Федерации), проведение эндохирургической холецистэктомии или операции по поводу доброкачественного новообразования матки все равно позволит получить положительное влияние на бюджет. А при сокращении расходов на случай лечения до 41,3% от исходного (что соответствует ситуации в 75% субъектов РФ) увеличению объема финансирования будет способствовать выполнение всех оперативных вмешательств из числа включенных в модель, кроме операций по поводу варикозного расширения вен или по поводу неосложненной грыжи передней брюшной стенки (варианты с наименьшим размером финансирования одного случая лечения).
Результаты анализа чувствительности модели к изменению частоты применения рокурония бромида показали, что при увеличении частоты с 12% (в исходной модели) до 25% для внедрения использования сугаммадекса потребуется дополнительное финансирование в размере 1 824 882 руб. в год. Благодаря внедрению сугаммадекса при такой частоте использования рокурония бромида общая экономия времени увеличится вдвое - до 145 часов в год. Это в конечном итоге позволит также вдвое увеличить финансирование за счет выполнения дополнительных операций (например, при выполнении в освободившееся время эндохирургической холецистэктомии – до 4 275 476 руб. в год).
Обсуждение
Согласно результатам моделирования, применение сугаммадекса с позиции системы здравоохранения приводит к снижению числа случаев остаточного НМБ. С позиции медицинской организации (стационара) применение сугаммадекса позволяет сократить время проведения одной операции с применением миорелаксанта рокурония. Высвободившееся время можно использовать для проведения дополнительных операций, что будет способствовать повышению доступности медицинской помощи, возрастанию оперативной активности и увеличению объема финансирования стационара.
Наши результаты совпадают с результатами зарубежных исследований экономической целесообразности применения сугаммадекса для реверсии НМБ. Авторы обзора Fuchs-Buderetal., 2012 [30], обобщившие результаты большей части выполненных экономических исследований, отмечают, что имеющиеся данные позволяют говорить о потенциальной возможности увеличения потока пациентов благодаря сокращению времени выхода из НМБ после анестезии, при этом повышение доходности работы больницы в денежном выражении может быть различным и зависит от особенностей организации работы операционных и эффективности управления ими. В то же время все авторы отмечают, что существует дефицит данных, характеризующих реальную практику проведения анестезии; в частности, точно неизвестна частота осложнений остаточного НМБ и их ресурсоемкость/ затратность, вследствие чего во всех модельных исследованиях использовалось значительное число допущений.
Таблица 6. Изменения бюджета стационара при сокращении размера возмещения расходов до 29%, 35% и 41,3% от исходного значения, заложенного в модель (на отдельный случай лечения хирургического больного)
| Дополнительный случай лечения | Изменение бюджета при сокращении размера возмещения расходов на отдельный случай лечения, руб.: | ||
|---|---|---|---|
| до 29% от исходного (охватывает 25% субъектов РФ) |
до 35% от исходного (охватывает 50% субъектов РФ) |
до 41,3% от исходного (охватывает 75% субъектов РФ) |
|
| Холецистэктомия |
-17 289 |
117 009 |
272 342 |
| Эндохирургическая холецистэктомия |
373 680 |
507 979 |
663 312 |
| Операция по поводу полипов носа |
-196 939 |
-59 964 |
98 464 |
| Операция по поводу неосложненной грыжи передней брюшной стенки |
-370 398 |
-273 118 |
-160 601 |
| Операция по поводу доброкачественного новообразования матки |
137 398 |
232 527 |
342 554 |
| Операция по поводу варикозного расширения вен |
-507 510 |
-418 119 |
-314 727 |
| Операция по поводу аденомы предстательной железы |
-12 313 |
122 955 |
279 409 |
Наше исследование тоже представляет собой модель, основанную на ряде допущений, обусловленных дефицитом данных. Допущения в нашей модели связаны, главным образом, с особенностями финансирования отечественного здравоохранения. Это, прежде всего, вариабельность методов оплаты и тарифов на оказание медицинской помощи. Если метод оплаты оказания стационарной помощи не стимулирует повышение оборота койки (оплата по смете или за койко-день), то больница не имеет прямой заинтересованности в увеличении числа проведенных операций и количества пролеченных больных. Однако с 2013 г. эти методы оплаты не должны использоваться, и все стационары переходят на оплату по законченному случаю, что стимулирует повышение интенсивности работы. Что касается вариабельности в уровнях финансирования здравоохранения между регионами, то она очень высока: разброс между минимальной и максимальной стоимостью койко-дня составлял в 2011 г. от 739 до 6409 руб. Очевидно, что при невысоком финансировании больнице сложнее компенсировать расходы на приобретение сугаммадекса за счет повышения оперативной активности. Тем не менее в анализе чувствительности мы показали, что даже при снижении тарифа на случай лечения хирургического больного до 29% от исходного значения (что может иметь место примерно в четверти субъектов РФ) стационар имеет возможность получить дополнительное финансирование, проводя в высвободившееся время операции с максимальным уровнем возмещения ( например, эндохирургическую холецистэктомию или операцию по поводу доброкачественного новообразования матки).
Также следует учитывать, что в практике наблюдаются вариации в доле операций, выполняемых с применением рокурония, в организации работы операционных и в тактике ведения больных после операции. Наша модель предназначена для крупных стационаров (в модель заложено 5000 операций в год), в которых экстубация больных проводится в операционной. Доля операций с использованием рокурония в нашей модели небольшая (12% от всех операций с использованием стероидных деполяризующих миорелаксантов), при ее увеличении будет увеличиваться и сэкономленное время работы операционных.
Мы основывали модель на допущении, что после операции в отсутствие осложнений большая часть больных (80%) переводится в профильное отделение, минуя ОРИТ. Такие больные поступают в ОРИТ при развитии осложнений остаточного НМБ, что приводит к дополнительным расходам стационара, но их абсолютный размер, как показали наши расчеты, невелик. Основная выгода ожидается от рационального использования высвободившегося времени операционной. Поэтому наша модель применима даже для стационаров, рутинно помещающих больных в ОРИТ после операции (в этих случаях лечение осложнений остаточного НМБ может и не привести к осязаемым дополнительным расходам).
Наконец, необходимо признать, что сокращение времени пребывания больного в операционной не является достаточным условием для интенсификации работы операционного блока и увеличения оперативной активности стационара. Очевидно, требуется и рациональное планирование работы (в частности, составление графика операций таким образом, чтобы время, необходимое для выполнения дополнительного вмешательства, высвобождалось бы в рамках одного дня). С этой точки зрения наша модель показывает потенциальные возможности, открывающиеся перед стационаром, реализовать которые можно при соблюдении определенных условий.
Выводы
1. В стационаре, выполняющем 5000 хирургических операций в год, ожидается 160 операций под общей анестезией с ИВЛ с использованием рокурония, в 99 из них в текущей практике восстановление НМП происходит спонтанно, в 61 - для реверсии НМБ используется неостигмин + атропин. Во всех этих случаях можно использовать сугаммадекс для более быстрой и безопасной реверсии НМБ.
2. Применение сугаммадекса позволит данному стационару:
- сократить число случаев остаточного НМБ в 15 раз (с 78 до 5 случаев в год);
- предупредить как минимум один случай внепланового поступления больного из операционной в ОРИТ в течение года;
- освободить 70 часов занятости операционной в год.
3. Применение сугаммадекса для 160 операций потребует дополнительного финансирования в размере 881 938 руб. в год за счет следующих изменений в расходах:
- закупка препарата сугаммадекс (в количестве, необходимом для обеспечения реверсии НМБ всем больным, получавшим рокуроний) - 1 078 739 руб. в год;
- исключение расходов на использования неостигмина с атропином у 61 больного - 410 руб. в год;
- исключение расходов на кислород для обеспечения ИВЛ в период восстановления НМП - 188 879 руб. в год;
- исключение расходов на оказание медицинской помощи в ОРИТ в случае развития осложнений НМБ - 7513 руб. в год.
4. Время, освободившееся в результате использования сугаммадекса, может быть использовано для проведения дополнительных операций (70 операций в год длительностью 60 мин и менее), что выражается в возможности получить дополнительное финансирование, объем которого будет зависеть от вида оперативных вмешательств, выполненных в освободившееся время, и составит:
- при выполнении холецистэктомии - 1 674 807 руб. в год;
- эндохирургической холецистэктомии - 2 065 777 руб. в год;
- операции по поводу полипов носа - 1 528 878 руб. в год;
- операции по поводу неосложненной грыжи передней брюшной стенки - 855 284 руб. в год;
- операции по поводу доброкачественного новообразования матки - 1 335 969 руб. в год;
- операции по поводу варикозного расширения вен - 618 780 руб. в год;
- операции по поводу аденомы предстательной железы - 1 691 998 руб. в год.
5. В итоге при рациональном управлении работой операционных на уровне стационара не только окупаются затраты на применение сугаммадекса, но и ожидается за счет увеличения числа проведенных операций получение дополнительного финансирования в размере от 855 тыс. до 2,1 млн руб. в год в зависимости от вида оперативных вмешательств, которые будут выполняться в освободившееся время.
6. Анализ чувствительности результатов расчетов к колебаниям расценок на оказание медицинской помощи показал, что даже при уменьшении размера возмещения расходов стационара (тарифов) на случаи хирургического лечения до 29% от исходного значения, заложенного в модель, можно за счет увеличения числа проведенных операций ожидать дополнительного финансирования при выполнении отдельных видов оперативных вмешательств, например, эндохирургической холецистэктомии и операции по поводу доброкачественного новообразования матки.
7. Анализ чувствительности результатов расчетов к колебаниям частоты использования рокурония показал, что при ее увеличении с 12% (в исходной модели) до 25% для внедрения использования сугаммадекса потребуется дополнительное финансирование в размере 1 824 882 руб. в год. Благодаря внедрению сугаммадекса общая экономия времени увеличится вдвое - до 145 часов в год. Это в конечном итоге позволит также вдвое увеличить объем финансирования за счет выполнения дополнительных операций (например, при выполнении в освободившееся время эндохирургической холецистэктомии - до 4 275 476 руб. в год).
Литература:
1. Berg H., Roed J., Viby-Mogensen J., et al. Residual neuromuscular block is a risk factor for postoperative pulmonary complications. A prospective, randomized, and blinded study of postoperative pulmonary complications after atracurium, vecuronium and pancuronium. Acta Anaesthesiol Scand. 1997; 41: 1095-1103.
2. Eikermann M., Groeben H., Husing J., Peters J. Accelerometry of adductor pollicis muscle predicts recovery of respiratory function from neuromuscular blockade. Anesthesiology. 2003; 98 (6): 1333-1337.
3. Eriksson L.I. Reduced hypoxic chemosensitivity in partially paralyzed man. A new property of muscle relaxants? Acta Anaesthesiol Scand. 1996; 40: 520-523.
4. Murphy G.S., Szokol J.W., Franklin M., Marymont J.H., Avram M.J., Vender J.S. Postanesthesia care unit recovery times and neuro-muscular blocking drugs: a prospective study of orthopedic surgical patients randomized to receive pancuronium or rocuronium. Anesth Analg. 2004; 98: 193-200.
5. Murphy G.S., Szokol J.W., Marymont J.H., Greenberg S.B., Avram M.J., Vender J.S. Residual neuromuscular blockade and critical respiratory events in the postanesthesia care unit. Anesth Analg. 2008; 107: 130-137.
6. Sundman E., Witt H., Olsson R., Ekberg O., Kuylenstierna R., et al. The incidence and mechanisms of pharyngeal and upper esophageal dysfunction in partially paralyzed humans: pharyngeal videoradiography and simultaneous manometry after atracurium. Anesthesiology. 2000; 92 (4): 977-984.
7. Fink H., Hollmann M.W. Myths and facts in neuromuscular pharmacology. New developments in reversing neuromuscular blockade. Minerva Anestesiol. 2012; 78 (4): 473-482.
8. Di Marco P., Della Rocca G., Iannuccelli F., Pompei L., Reale C., Pietropaoli P. Knowledge of residual curarization: an Italian survey. Acta Anaesthesiol Scand. 2010; 54 (3): 307-312. doi: 10.1111/j.1399-6576.2009.02131.x. Epub 2009 Oct 15.
9. Murphy G.S., Brull S.J. Residual neuromuscular block: lessons unlearned. Part I: definitions, incidence, and adverse physiologic effects of residual neuromuscular block. AnesthAnalg. 2010 Jul; 111 (1): 120-128.
10. Грачев С.С. и др. Мониторинг нейромышечного блока в анестезиологии: учебно-методическое пособие. Минск: БГМУ; 2012. - 23 с.
11. Кириенко П.А., Гриненко Т.Ф., Борзенко А.Г., Гельфанд Б.Р. Новые мышечные релаксанты в клинической анестезиологии. Consilium Medicum. 2001; т. 3, №7 - Приложение.
12. Grosse-Sundrup M., Henneman J.P., Sandberg W.S., Bateman B.T., et al. Intermediate acting non-depolarizing neuromuscular blocking agents and risk of postoperative respiratory complications: prospective propensity score matched cohort study. BMJ2012; 345: e6329 doi: 10.1136/bmj.e6329
13. Султанов Л.Р., Баялиева А.Ж., Шпанер Р.Я. Остаточная нейро-мышечная блокада и методы ее нейтрализации. Казанский медицинский журнал. 2011; 92, № 3: 426-429.
14. Кириенко П.А., Горобец Е.С., Бабаянц А.В., Проценко Д.Н., Смирнов Г.А., Шмаков И.А., Гельфанд Б.Р. Неадекватная миоплегия и остаточная кураризация - значимость проблемы с точки зрения анестезиолога и хирурга. Анестезиология и реаниматология. 2011; №5: 35-38.
15. Петриков С.С., Солодов А.А., Тимербаев В.Х., Ефременко С.В., Голубев В.А., Комардина Е.В., Крылов В.В. Остаточный нейро-мышечный блок после применения миорелаксантов у нейрохирургических больных. Частота развития, диагностика и реверсия. Анестезиология и реаниматология. 2012; выпуск 4: 73-75.
16. Султанов Л.Р. Сравнительная оценка остаточной кураризации при нейрохирургических вмешательствах в раннем послеоперационном периоде с помощью акцелеромиографии / Р.Я. Шпанер. Тезисы докладов XIII Всероссийской конференции «Жизнеобеспечение при критических состояниях», посвященной 75-летию НИИ общей реаниматологии им. В.А. Неговского РАМН. Москва. 2011: 153.
17. Рекомендации по диагностике и реверсии остаточного нейро-мышечного блока в нейрохирургии. Вестникинтенсивнойтерапии. 2011; №4: 52-62.
18. Abrishami A., Ho J., Wong J., Yin L., Chung F. Sugammadex, a selective reversal medication for preventing postoperative residual neuromuscular blockade. Cochrane Database Syst Rev. 2009; 7 (4): CD007362.
19. Chambers D., Paulden M., Paton F., Heirs M., Duffy S., Craig D., Hunter J., Wilson J., Sculpher M., Woolacott N. Sugammadex for the reversal of muscle relaxation in general anaesthesia: a systematic review and economic assessment. Health Technol Assess. 2010 Jul; 14 (39): 1-211.
20. Zhang B., Menzin J., Tran M.H., Neumann P.J., Friedman M., Sussman M., Hepner D. The potential savings in operating room time associated with the use of sugammadex to reverse selected neuro-muscular blocking agents: findings from a hospital efficiency model. Value in Health. 2008; 11 (3): A244.
21. Grintescu I., Mirea L., Ologoiu D., Ungureanu R., Mekauvar S., et al. Comparison of the cost-effectiveness of sugammadex and neo-stigmine during general anesthesia for laparoscopic cholecystectomy. Br J Anaesth. 2009; 103 (6): 917P.
22. Baumgart A., Denz C., Bender H., et al. Simulation-based analysis of novel therapy principles. Effects on the efficiency of operating room processes (in German). Anaesthesist. 2009; 58: 180-186.
23. Raft J., Chenot E.-D., Longrois D., Meistelman C. Analysis of neu-romuscular blocking drugs and sugammadex expenses, one year after its introduction in routine clinical practice (letter, in French). Ann Fr Anesth Reanim. 2011; 30: 758-759.
24. Ledowski T., Hillyard S., Kozman A., Johnston F., Gillies E., Greenaway M., Kyle B.C. Unrestricted access to sugammadex: impact on neuromuscular blocking agent choice, reversal practice and associated healthcare costs. Anaesth Intensive Care. 2012; 40 (2): 340-343.
25. Watts R.W., London J.A., van Wijk R.M., Lui Y.L. The influence of unrestricted use of sugammadex on clinical anaesthetic practice in a tertiary teaching hospital. Anaesth Intensive Care. 2012; 40 (2): 333-339.
26. Paton F., Paulden M., Chambers D., et al. Sugammadex compared with neostigmine/glycopyrrolate for routine reversal of neuromus-cular block: a systematic review and economic evaluation. Br J Anaesth. 2010; 105: 558-567.
27. Chambers D., Paulden M., Paton F., et al. Sugammadex for reversal of neuromuscular block after rapid sequence intubation: a systematic review and economic assessment. Br J Anaesth. 2010; 105: 568-575.
28. Chambers D., Paulden M., Paton F., Heirs M., Duffy S., Craig D., Hunter J., Wilson J., Sculpher M., Woolacott N. Sugammadex for the reversal of muscle relaxation in general anaesthesia: a systematic review and economic assessment. Health Technol Assess. 2010 Jul; 14 (39): 1-211.
29. Insinga R.P., Lundberg J. Economic Impact of using sugammadex for the reversal of deep neuromuscular blockade in the Swedish health care setting. Value in Health. 2012; 15 (4): р. A74.
30. Fuchs-Buder T., Meistelman C., Schreiber J.U. Is sugammadex economically viable for routine use. Curr Opin Anaesthesiol. 2012; 25 (2): 217-220.
31. Sabo D., Jones R.K., Berry J., Sloan T., Chen J.Y., et al. Residual neuromuscular blockade at extubation: A randomized comparison of sugammadex and neostigmine reversal of rocuronium-induced blockade in patients undergoing abdominal surgery. Journal of Anesthesia & Clinical Research. 2011; 2 (6).
32. Hayes A.H., Mirakhur R.K., Breslin D.S., Reid J.E., McCourt K.C. Postoperative residual block after intermediate-acting neuromuscular blocking drugs. Anaesthesia. 2001; 56 (4): 312-318.
33. Dahl V., Pendeville P.E., Hollmann M.W., Heier T., Abels E.A., et al. Safety and efficacy of sugammadex for the reversal of rocuronium-induced neuromuscular blockade in cardiac patients undergoing noncardiac surgery. Eur J Anaesthesiol. 2009; 26 (10): 874-884.
34. Butterly A., Bittner E.A., George E., Sandberg W.S., Eikermann M., et al. Postoperative residual curarization from intermediate-acting neuromuscular blocking agents delays recovery room discharge. Br J Anaesth. 2010; 105 (3): 304-309.
35. Haller G., Myles P.S., Wolfe R., Weeks A.M., Stoelwinder J., McNeil J. Validity of unplanned admission to an intensive care unit as a measure of patient safety in surgical patients. Anesthesiology. 2005; 103 (6): 1121-1129.
36. Haller G., Myl es P.S., Langley M., Stoelwinder J., McNeil J. Assessment of an unplanned admission to the intensive care unit as a global safety indicator in surgical patients. Anaesth Intensive Care. 2008; 36 (2): 190-200.
37. Piercy M., Lau S., Loh E., Reid D., Santamaria J., Mackay P. Unplanned admission to the intensive care unit in postoperative patients - an indicator of quality of anaesthetic care? Anaesth Intensive Care. 2006; 34 (5): 592-598.
38. Eichenberger A.S., Haller G., Cheseaux N., Lechappe V., Garnerin P., Walder B. A clinical pathway in a post-anaesthesia care unit to reduce length of stay, mortality and unplanned intensive care unit admission. EurJAnaesthesiol. 2011; 28 (12): 859-866.
39. Практикум по анестезиологии для интернов. 2-е издание, переработанное и дополненное. Под ред. Ю.С. Полушина. Санкт-Петербург; 2002 г. - 178 с.
40. Тарифное соглашение на медицинские услуги, оказываемые по территориальной программе обязательного медицинского страхования города Москвы.
41. Клинико-экономический анализ. Под ред. П.А. Воробьева. М.: Ньюдиамед; 2008.
7 Согласно методике, принятой при использовании тарифов системы ОМС, для анализа результатов оценки затрат на оказание медицинской помощи использован поправочный коэффициент, равный 1,86, позволяющий учесть финансирование из других источников (кроме бюджета ОМС, финансовые нормативы которого лежат в основе расчета затрат) [41].
- Войдите или зарегистрируйтесь, чтобы получить возможность отправлять комментарии