| Новости | e-Образование | Врачебные Общества | Тематические группы | Библиотека | Медиатека | Мероприятия | Атлас |
Присоединяйтесь!
- Повышение квалификации
- Сертифицированное образование
- Актуальные статьи
- Обзоры и репортажи
- Клинические случаи
- Новости медицины
- Советы коллег
Сообщество: Оценка Медицинских Технологий
Современный алгоритм ОМТ на примере различных методов лечения больных раком предстательной железы
А.В. Гажева, Е.А. Крекнина
ФГБУ «Центральный научно-исследовательский институт организации и информатизации здравоохранения» Министерства здравоохранения Российской Федерации, Москва, Россия
Современный алгоритм оценки медицинских технологий на примере различных видов хирургических, малоинвазивных и комбинированных методов лечения больных локализованным и местно-распространенным раком предстательной железы
Современный этап развития здравоохранения характеризуется внедрением большого количества дорогостоящих инновационных технологий. Лечение рака предстательной железы (РПЖ) уже невозможно без методов брахитерапии, высокочастотного ультразвука и гормональных препаратов. Затраты на данные технологии составляют десятки миллионов рублей, поэтому без клинико-экономической оценки говорить о том, какие из них могут использоваться повсеместно, а какие должны остаться на уровне клинических институтов, невозможно. В статье представлены результаты оценки технологий диагностики и лечения локализованного и местно-распространенного РПЖ с использованием алгоритма, внедренного в практику ЦНИИ организации и информатизации здравоохранения Минздрава России. Сформированы рекомендации по применению различных методов лечения РПЖ с учетом результатов оценки.
Введение
Среди комплекса социально значимых болезней злокачественные новообразования занимают лидирующие позиции в снижении потенциала здоровья и продолжительности жизни населения. Ведущей локализацией в структуре мужской онкопатологии является рак предстательной железы (РПЖ). Затраты на диагностику и различные виды лечения РПЖ возрастают стремительно в связи с внедрением инновационных медицинских технологий. Прямые затраты на лечение РПЖ в зарубежных странах освещаются в литературе в достаточном объеме [1]. Однако российских исследований по комплексной оценке медицинских технологий, затрагивающих все этапы развития заболевания, недостаточно. Разработка унифицированного алгоритма проведения оценки медицинских технологий (ОМТ) - актуальная и своевременная задача. Внедрение клинико-экономического анализа в систему российского здравоохранения позволит качественно и оперативно рассчитывать экономическое бремя потерь от онкологической патологии в масштабе страны, внедрять в рутинную практику регионов прошедшие отбор современные и экономически обоснованные методы лечения и осуществлять комплексную ОМТ.
Материалы и методы
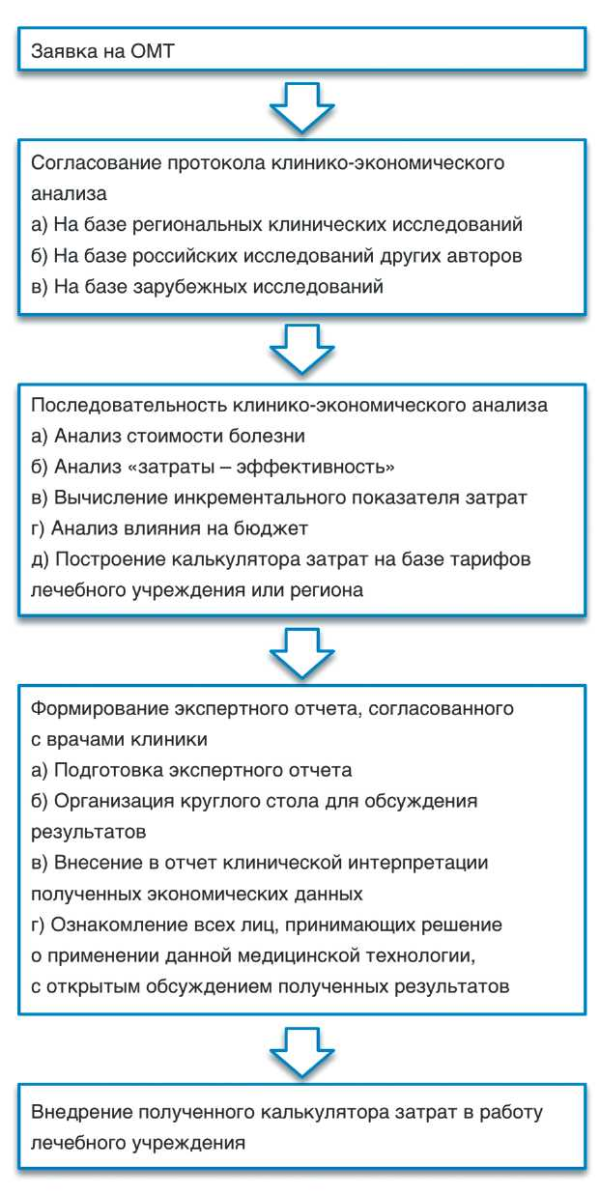
Нами проведено исследование по ОМТ диагностики и лечения локализованного и местно-распространенного РПЖ с использованием алгоритма, внедренного в практику ЦНИИ организации и информатизации здравоохранения Минздрава России (рис. 1). На наш взгляд, основной задачей ОМТ на уровне клинического института, лечебного учреждения или регионального министерства здравоохранения является решение конкретного вопроса, связанного с оценкой технологий при определенной патологии, которая должна носить прикладной характер, т.е. использоваться в процессе формирования бюджета на обеспечение соответствующей группы пациентов. При этом одной из самых трудных задач остается выбор социально значимой патологии и согласование протокола клинического исследования, на базе которого проводится экономическая оценка. Популяция больных должна соответствовать тому региону, в котором проводится ОМТ, обладая сходными демографическими и региональными характеристиками [2].
Исследование проводилось в четыре этапа. Первый этап, эпидемиологический, - анализ заболеваемости урологическими злокачественными новообразованиями (ЗНО) с 2001 по 2011 гг. С одной стороны, эпидемиологические показатели заболеваемости и распространенности онкологической патологии за прошедшее десятилетие отражают неуклонный рост, что связано с увеличением доли пожилого населения и с более ранней выявляемостью заболеваний современными методами диагностики. С другой стороны, наблюдается недостаток эффективности системы профилактики и предотвращения заболеваний. Анализ статистической информации позволяет констатировать, что РПЖ имеет наибольшие темпы роста заболеваемости и смертности по сравнению с другими урологическими ЗНО. Заболеваемость РПЖ (68,1 на 100 000 населения) в 2011 г. превышала уровень заболеваемости ЗНО мочевого пузыря (53,8), при этом годовой прирост опухолей предстательной железы был втрое выше годового прироста опухолей мочевого пузыря (+13,5% и +4,5% соответственно). За период 2001-2011 гг. «грубый» показатель смертности мужского населения от ЗНО предстательной железы вырос на 59,9% [4].
Второй этап, клинический - разработка и согласование протокола клинического исследования, в которое вошло 525 пациентов c локализованной и местно-распространенной формой. Хирургическое лечение проведено методами открытой радикальной простатэктомии и лапароскопической радикальной простатэктомии. Малоинвазивные методики представлены брахитерапией и методом высокочастотного ультразвука (HIFU), которыми пролечено 183 пациента. Консервативные методы лечения представлены конформной дистанционной лучевой терапией (ДЛТ), которая проведена 105 пациентам, и гормональной терапией, которую получили 107 пациентов.
При локализованном и местно-распространенном РПЖ объем необходимых исследований включал в себя исследование клинических анализов крови и мочи, биохимического анализа крови, определение электролитного состава сыворотки крови, определение группы крови и резус-принадлежности, исследование состояния свертывающей системы крови, определение антител к вирусу иммунодефицита человека 1-го и 2-го типов, антител, суммарных к возбудителю сифилиса, поверхностного антигена вируса гепатита В (HBsAg) и антител, суммарных к вирусу гепатита С (Anti-HCV), ЭКГ.
Рис. 1. Алгоритм проведения и внедрения оценки медицинских технологий в работу регионального министерства здравоохранения или лечебного учреждения.
Длительность госпитализации для лечения с применением различных медицинских технологий рассчитывалась по изданию «Алгоритмы объемов диагностики и лечения злокачественных новообразований» под редакцией академика РАМН В.И. Чиссова: до лечения - 5-7 дней, при выполнении операции - 21 день, т. е. суммарный расчетный срок госпитализации для группы хирургического лечения был принят равным 28 дням [5]. Для группы, которой выполнена ДЛТ, планируемая суммарная очаговая доза (СОД) составляла 70 Гр, но не у всех больных удалось довести дозу до планируемого значения вследствие развития побочных реакций и осложнений. Минимальная СОД облучения составила 48 Гр, максимальная - 74 Гр; длительность лечения - 46 дней. Среднее время проведения терапии малоинвазивными методами лечения, такими как брахитерапия и метод высокоинтенсивного ультразвука (HIFU), составляла 46-47 дней. Средняя длительность лечения при применении мало-инвазивных методов составила от 4 до 10 дней.
Наличие клинически локализованного РПЖ служило показанием для оперативных вмешательств. При открытой радикальной простатэктомии применялась стандартная позадилонная техника. Для выполнения лапароскопической простатэктомии был выбран ее ретроперитонеоскопический вариант по стандартной антеградной методике. При этом использовали стандартный набор эндохирургического оборудования.
Брахитерапия проводилась с использованием связанных полиглактиновой нитью микроисточников систем I125Rapid-Strand (Amersham, Великобритания) и IsoCord (Bebig, Германия). Планирование оптимального расположения радиоактивных источников внутри предстательной железы на основании изображения, полученного при трансректальном ультразвуковом исследовании простаты, выполнялось с помощью специального программного обеспечения PSID 4.1 (D&K Technologies, США) и Vari'Seed 7.1 (Varian, США). Микроисточники содержали радионуклиды I с периодом полураспада 59,4 дня. Количество имплантированных одному пациенту микроисточников варьировалось от 38 до 280 штук. Оценку расположения зерен после имплантации проводили с помощью УЗИ или рентгеновского изображения. Планиметрический контроль качества имплантации выполняли на 30-е сутки с помощью мультиспиральной компьютерной томографии.
HIFU проводился на аппарате Sonablate 500 (FocusSurgery, США) по стандартной методике. С целью подготовки к проведению HIFU у 19 больных (33%) была выполнена трансуретральная резекция (ТУР) предстательной железы, показаниями для которой служили объем простаты более 40 см3 и/или переднезадний размер более 4 см.
Третий этап, экономический - проведение экономического анализа представленных технологий диагностики и лечения [3]. По итогам клинико-экономической части разработан калькулятор затрат на лечение РПЖ, позволяющий оценить экономическое бремя каждой из исследованных технологий. Калькулятор дает возможность использовать тарифы на оказание медицинской помощи и цены лекарственных средств и расходных материалов в зависимости от региональных особенностей.
Четвертый этап, практический - внедрение экономического калькулятора по расчету экономического бремени лечения РПЖ в практику лечебных онкологических учреждений и презентация его практической необходимости.
В исследовании использованы все доступные методы фармакоэкономического анализа: анализ стоимости болезни, анализ «затраты - эффективность» с вычислением инкрементальных (дополнительных) затрат на единицу эффективности, сформирован калькулятор затрат на представленные технологии. Исследование проводилось в соответствии с требованиями Приказа МЗ РФ «Об утверждении отраслевого стандарта «Клинико-экономические исследования. Общие положения» от 27 мая 2002 г. №163, а также с рекомендациями современных отечественных и зарубежных руководств по проведению клинико-экономического анализа.
Результаты анализа стоимости болезни приведены в виде прямых медицинских затрат на диагностические, лечебные, реабилитационные и профилактические медицинские услуги. В рамках анализа «затраты - эффективность» проводился расчет соотношения затрат на единицу эффекта (в нашем случае - на достижение 5-летней выживаемости без прогрессирования заболевания).
Результаты и обсуждение
При сравнении периоперационных параметров наилучшие результаты продемонстрировала брахитерапия. Это и непродолжительное время оперативного вмешательства и послеоперационного дренирования мочевого пузыря, и небольшая длительность стационарного лечения, и отсутствие кровопотери и необходимости в гемотрансфузии, и минимальное проявление послеоперационной боли. Несколько хуже эти показатели проявились при HIFU, однако данный метод превосходил оба варианта радикальной простатэктомии по периоперационным результатам, кроме времени на выполнение оперативного вмешательства. Так как данное время для HIFU включало еще и время на выполнение подготовительных операций, общее время при HIFU было сопоставимым с открытой простатэктомией, но достоверно короче, чем время для лапароскопической операции. Кроме операционного времени открытая радикальная простатэктомия другого преимущества перед лапароскопической операцией не имела. По частоте гемотрансфузий и количеству больных с осложнениями методики радикальной простатэктомии между собой достоверного различия не показали, а по срокам дренирования, срокам стационарного лечения и проявлениям послеоперационной боли лапароскопическая простатэктомия имела преимущество перед открытой операцией.
Хирургические методы лечения, такие как открытая радикальная простатэктомия и лапароскопическая радикальная простатэктомия показали в нашем исследовании 5-летнюю безрецидивную выживаемость 80% и 77,6% соответственно. Преимущество радикальной простатэктомии в безрецидивной выживаемости было более выражено в группах больных местно-распространенным РПЖ с уровнем простат-специфического антигена более 20 нг/мл и при низкой дифференцировке опухоли. Малоинвазивная методика брахитерапии по отдаленным результатам лечения показала 5-летнюю безрецидивную выживаемость 79%, что сопоставимо с результатами радикальной простатэктомии. Метод HIFU показал 5-летнюю выживаемость на уровне 75,3%, что также является сопоставимым результатом с хирургическими методиками лечения.
При противопоказаниях к хирургическому лечению методом выбора является конформная ДЛТ. У больных с низко дифференцированным РПЖ отмечено достоверное улучшение выживаемости без признаков клинического прогрессирования в группе ДЛТ (58,0%) по сравнению с группой гормональной терапии (41,9%).
Прямые затраты на постановку диагноза и определение показаний для хирургического или консервативного лечения больных локализованными стадиями РПЖ составили 14 200 руб. на пациента. Проведен анализ стоимости болезни по каждой технологии, который показал, что метод HIFU не только имеет высокую клиническую эффективность, но и экономичен. Затраты на оказание помощи данным методом составили 64 010 руб. Однако на уровне внедрения метода в практику учреждения потребуются существенные затраты на закупку оборудования, такого как цистопический набор Karl Stolz стоимостью от 400 000 руб., комплект для ТУР Olympus стоимостью 3 900 000 руб. и аппарат для HIFU Sonablate 500 стоимостью 44 000 000 руб. В итоге, затраты на одну процедуру с учетом амортизационных отчислений, составят от 12 700 до 16 700 руб. на пациента.
Самым затратным методом является брахитерапия, прямые затраты на проведение метода составили 496 310 руб. Брахитерапия проводится радиоактивными препаратами зарубежного производства (I125Rapid-Stand, Англия; IsoCord, Германия), представляющими собой связанные полиглактиновой нитью микроисточники с радиоактивным йодом. Стоимость одного источника составляет 5000 руб., в среднем пациенту может быть необходимо от 50 до 280 источников, из чего и будет складываться основная стоимость лечения. В представленном расчете использовалось среднее количество микроисточников - 92 штуки. Кроме этого потребуется закупка дорогостоящего оборудования, такого как: программное обеспечение, стабилизатор, степпер с устройством крепления ультразвукового датчика, координатная решетка-трафарет, иглозарядная установка и УЗИ со специальными датчиками. Рыночная стоимость всего оборудования составляет более 22 млн руб., затраты на оборудование с учетом амортизационных отчислений - от 1195 до 2390 руб. на пациента.
Таким образом, по показателю «затраты/эффективность», рассчитанному на 5 лет безрецидивной выживаемости, метод высокочастотного ультразвука должен быть принят как наиболее выгодный. В случае появления российских разработок для брахитерапии стоимость препаратов может существенно снизиться, это приведет к тому, что метод брахитерапии будет не только самым эффективным, но и менее затратным (табл. 1).
Тем больным, которым оперативные методики противопоказаны, был назначен один из видов консервативного лечения. Кроме степени распространения РПЖ значительную роль при выборе тактики лечения играет прогноз по степеням риска. Так, при хорошем прогнозе с низкой степенью риска может быть использована только конформная ДЛТ, однако при умеренном и плохом прогнозе к ДЛТ необходимо подключать гормональную терапию антиандрогенами (АА) или аналогами лютеинизирующего рилизинг-гормона (ЛГРГ). Для проведения гормональной терапии используются три основных лекарственных метода: терапия агонистами ЛГРГ, максимальная андрогенная блокада (МАБ) - комбинация агонистов ЛГРГ и антиандрогенов - и монотерапия антиандрогенами.
Наиболее распространенными АА для проведения гормональной терапии являются бикулатамид и флутамид, в РФ зарегистрировано более шести их торговых наименований как зарубежного, так и отечественного производства. Аналоги ЛГРГ, которые широко применяются в РФ, это гозерелин, трипторелин, лейпрорелин и бусерелин. Препараты ЛГРГ выпускаются в пролонгированных формах, причем один из них, лейпрорелин, - в 6-месячной форме, поэтому стоимость терапии будет зависеть от выбранного лекарства и его формы выпуска.
Таким образом, для больных с хорошим прогнозом и низкой степенью риска независимо от степени распространения опухоли стоимость терапии будет равна 120 610 руб. (стоимость курса ДЛТ). Комбинация конформной ДЛТ с любым из методов гормональной терапии приведет к увеличению прямых затрат на стоимость лекарственных препаратов. Исходя из данных реестра, для каждого препарата была рассчитана средняя оптовая цена с учетом НДС.
Стоимость гормональной терапии по схеме МАБ составила 123 852 руб. на одного пациента в год. Стоимость лечения препаратами ЛГРГ составила 104 267 руб. в год. Стоимость лечения в режиме монотерапии АА составила 108 921,64 руб. в год. При использовании АА в комбинации затраты составят 229 531,10 руб., при комбинации АА с ЛГРГ -224 877,0 руб. на человека (табл. 2).
Гормональную терапию в монорежиме необходимо проводить при наличии противопоказаний к хирургическому лечению и отсутствии возможности использования малоинвазивного лечения, так как выживаемость больных без клинического прогрессирования при проведении гормонотерапии достоверно хуже, чем при радикальной простатэктомии.
Как видно из табл. 3, по показателям «затраты/эффективность» любая из медицинских технологий при местно-распространенной стадии РПЖ существенно хуже хирургических или малоинвазивных методик. Это еще раз подчеркивает значимость своевременного выявления больных РПЖ на ранних стадиях, когда затраты на лечение, понесенные государством, могут дать максимальный эффект для пациента.
Таблица 1. Прямые затраты и показатели «затраты/эффективность» для различных методов лечения РПЖ
| Показатель | Открытая простатэктомия | Лапароскопическая простатэктомия | Бахитерапия | HIFU |
| Затраты на оказание медицинской помощи одному больному, руб. | 105 010,00 | 110 510,00 | 496 310,00 | 64 010,00 |
| Показатель «затраты/эффективность», руб. на случай 5-летней выживаемости без прогрессирования |
131 262,50 |
142 409,79 |
628 240,51 |
85 006,64 |
Таблица 2. Прямые затраты на лечение в зависимости от степени риска и прогноза РПЖ
| Прогноз | Степень риска | Вид терапии | Затраты, руб. |
| Хороший | Низкий | ДЛТ | 120 610,00 |
| Умеренный | Средний | ДЛТ + гормональная терапия (антиандрогены) | 229 531,10 |
| Плохой | Высокий | ДЛТ + гормональная терапия (ЛГРГ) | 224 877,00 |
Таблица 3. Показатель «затраты/эффективность» для комбинированной и лучевой терапии по сравнению с ЛГРГ
| Показатель | ДЛТ + гормональная терапия | ДЛТ | ЛГРГ |
| Затраты на оказание медицинской помощи одному больному, руб. | 224 877 | 120 610 | 104 267 |
| Показатель «затраты/эффективность», руб. на случай 5-летней выживаемости без прогрессирования | 387 718 | 207 948 | 254 309 |
Кроме фармакоэкономических показателей проведен анализ структуры затрат. В структуре общих затрат при лечении оперативным методом госпитализация занимает 54%, операция - 28% и диагностика - 18%. При использовании метода ДЛТ госпитализация составляет 59% затрат, ДЛТ - 29% и диагностика - 12% в общей структуре затрат. В структуре затрат на любой из видов гормональной терапии (МАБ, монотерапия антиандрогенами или монотерапия ЛГРГ) диагностика занимает от 8 до 12%, остальное - затраты на лекарственные препараты. Учитывая, что гормональная терапия проводится амбулаторно, затрат на госпитализацию пациента нет. Структура затрат на методы брахитерапиии HIFU существенно отличается от других технологий в связи с высокой стоимостью оборудования для их проведения.
Заключение
При проведении ОМТ должны быть использованы международные принципы и алгоритмы, которые позволят сопоставить полученные локальные данные с международными экспертными оценками. ОМТ должна проводиться в несколько этапов. В ходе первого этапа на основе эпидемиологических данных проводится выбор социально значимой патологии. Второй этап - проведение клинического исследования для оценки эффективности применяемых и альтернативных технологий. Третий этап - проведение экономического анализа. Четвертый этап - внедрение полученных данных в лечебные учреждения, проводящие диагностику и лечение данной патологии.
Данные о клинической эффективности альтернативных медицинских технологий должны быть взяты из реальных российских клинических исследований, и только в случаях инновационных методов, которые недавно зарегистрированы в РФ, могут быть использованы данные зарубежных клинических исследований.
По результатам ОМТ метод HIFU можно признать малозатратным, затем в порядке уменьшения эффективности следуют открытая простатэктомия, лапароскопическая простатэктомия и брахитерапия. Существенным ограничением использования малоинвазивных методов брахитерапиии HUFU является высокая стоимость оборудования и расходных материалов. Малоинвазивные методы лечения, такие как брахитерапия и HIFU, показали высокую клиническую эффективность, отсутствие серьезных осложнений, лучшие данные по продолжительности манипуляций, меньшую по сравнению с открытой простатэктомией длительность госпитализации. Отсутствие значимых побочных эффектов позволяет рассматривать мало-инвазивные методы как наиболее экономически выгодные. Отечественным производителям необходимо наладить выпуск расходных материалов и препаратов для обеспечения данных технологий.
Выбирая гормонотерапию для группы больных с хорошим и умеренным прогнозом, мы высвобождаем место в стационаре и время работы лучевой установки, которая в обычных онкологических диспансерах испытывает серьезную загрузку, давая возможность проведения данного лечения пациентам с другими патологиями, где лекарственная терапия не может служить альтернативой.
Подводя итоги вышесказанному, необходимо еще раз подчеркнуть, что у ОМТ есть уникальные возможности в области содействия разработке политики здравоохранения, долгосрочному планированию, управлению и внедрению технологий. Ее нужно использовать как стратегический инструмент, позволяющий преодолеть разобщенность между лицами, принимающими решения, и практикующим здравоохранением, что позволит ОМТ приносить пользу в долгосрочном планировании и управлении здравоохранением при внедрении новых технологий.
Литература:
1. Зеленова О.В., Русаков И.Г., Болотина Л.В., Данилова Т.В., Быстров С.В. Обзор экономических затрат на различные методы лечения больных раком предстательной железы и качества жизни на основе зарубежного опыта. Фармакоэкономика. 2010; №4: 35-44.
2. Зеленова О. В. Методология, стратегия и модели применения клинико-экономического анализа для выбора оптимальных методов лечения пациентов (на примере онкоурологических заболеваний). Сборник работ I Международной итоговой научно-практической конференции «По страницам диссертаций 2012 года». Новосибирск, 2012; 17-20.
3. Зеленова О.В. Оценка медицинских технологий терапии рака предстательной железы современными методами клинико-экономического анализа. Паллиативная медицина и реабилитация. 2013; №1: 27-30.
4. Злокачественные новообразования в России в 2011 году (заболеваемость и смертность). Под редакцией В.И. Чиссова, В.В. Старинского, Г.В. Петровой. Москва, 2013 г.
5. Методические рекомендации: алгоритм объемов диагностики и лечения злокачественных новообразований. Под редакцией академика РАМН В.И. Чиссова. Москва, 2002 г.
- Войдите или зарегистрируйтесь, чтобы получить возможность отправлять комментарии